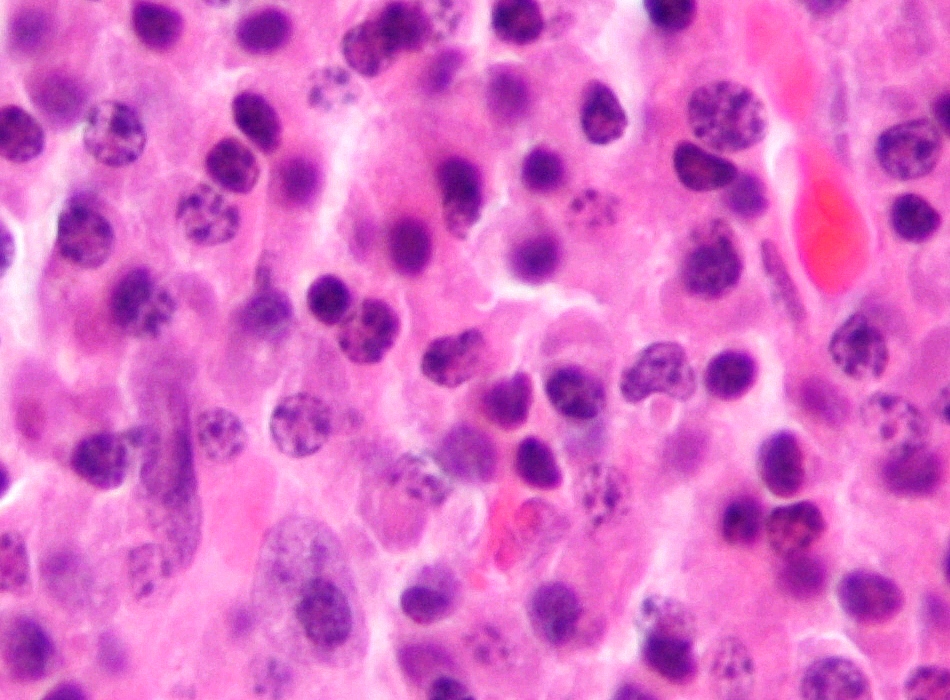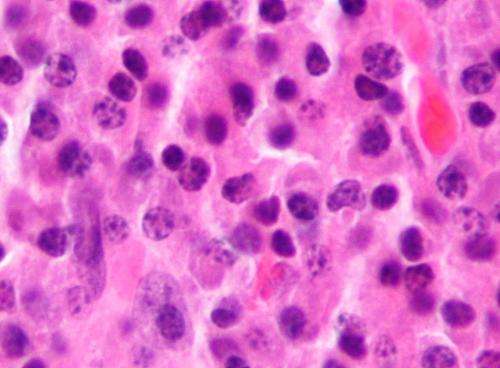
Micrografía de un plasmocitoma, correlato histológico del mieloma múltiple. Tinción H&E. Crédito: Wikipedia/CC BY-SA 3.0
Un esfuerzo sin precedentes para secuenciar el genoma, el exoma y el ARN en tumores de pacientes con mieloma múltiple define subtipos distintos de la enfermedad, según un equipo internacional de científicos dirigido por investigadores del Instituto de Investigación Genómica Traslacional (TGen), parte de City of Hope.
Los hallazgos del estudio observacional de 12 años brindan una imagen más clara de los cambios genéticos que pueden ser importantes en cada subtipo de este cáncer de células plasmáticas productoras de anticuerpos, que es tratable pero incurable. Esta información podría ayudar a orientar tratamientos más personalizados en el futuro, según los investigadores. escribir en Genética de la naturaleza.
Los científicos identificaron la base genética de una población de pacientes de alto riesgo, denominada «PR», que se asocia con una supervivencia media de menos de dos años en comparación con la supervivencia media en el estudio, que supera los ocho años. Alrededor del 25% de los pacientes pasaron al subtipo PR durante el estudio, y aquellos que pasaron al subtipo PR tuvieron peores resultados, con una supervivencia media de 88 días después de la transición.
«Conocemos este subtipo desde hace más de una década y ahora hemos demostrado que se trata de un grupo de pacientes de alto riesgo con las terapias que se utilizan hoy en día. Claramente, estos son pacientes a los que debemos incluir en ensayos clínicos porque los medicamentos actuales simplemente no funcionan para ellos», dijo Jonathan Keats, Ph.D., profesor adjunto, director del Centro de Bioinformática y Secuenciación Colaborativa en TGen y autor principal del artículo.
«Lo que demostramos claramente es que existe una base genética para que las personas pertenezcan al subgrupo PR».
El estudio también «ayuda a destacar que la enfermedad en etapa avanzada no es como la enfermedad en etapa temprana, y en una era en la que estamos avanzando hacia la detección temprana, los medicamentos que funcionan en la etapa temprana pueden no ser los mismos que funcionan en la etapa más avanzada», agregó Keats.
El estudio Relating Clinical Outcomes in Multiple Myeloma to Personal Assessment of Genetic Profile (CoMMpass) de la Multiple Myeloma Research Foundation (MMRF) incluyó a 1.143 pacientes de 84 centros clínicos ubicados en Estados Unidos, Canadá, España e Italia, inscritos entre 2011 y 2015 y que siguieron a los pacientes durante al menos ocho años después del diagnóstico.
Se trata del estudio de secuenciación individual más grande de pacientes con mieloma múltiple realizado hasta la fecha, basado en el número de pacientes y el número de ensayos de secuenciación realizados.
«También hay datos clínicos sobre estos pacientes recogidos cada tres meses a lo largo de toda la evolución de su enfermedad, no sólo cuando se les realiza el perfil genético, lo que constituye un auténtico tesoro», afirmó Keats.
Desde hace tiempo se conocen dos grupos principales de pacientes con mieloma múltiple: un grupo hiperdiploide con copias adicionales de cromosomas en las células tumorales y un grupo no hiperdiploide con reordenamientos cromosómicos. El enfoque utilizado por el equipo actual de investigadores les ayudó a identificar diferentes subgrupos dentro de estas amplias categorías.
«Muchos estudios han analizado un método (uno analiza el estado del número de copias y otro analiza si hay mutaciones), pero muy pocos integran los dos para comprender realmente cómo funciona un gen individual en ese paciente», señaló Keats. «Para este campo, hemos proporcionado una lista muy sólida de genes candidatos que son importantes en la enfermedad».
Keats dijo que los hallazgos podrían cambiar la forma en que los médicos hablan con sus pacientes sobre la elaboración de un plan de tratamiento. Aunque la creencia común es que los pacientes hiperdiploides tienen una supervivencia general más favorable, por ejemplo, los investigadores descubrieron que «hiperdiploide» abarca cinco grupos diferentes de pacientes, uno de los cuales tiene resultados significativamente peores y podría beneficiarse de una terapia agresiva.
Uno de los próximos retos es encontrar medicamentos compatibles con características genéticas específicas, afirmó Keats. «Hemos respondido claramente a la pregunta de qué tipos de fármacos existen, pero no a qué fármacos responden mejor».
TGen se basa en este trabajo pionero para ofrecer medicina personalizada a los pacientes con mieloma múltiple mediante el lanzamiento de la secuenciación completa del genoma de grado clínico en el laboratorio clínico de TGen. Esta prueba proporcionará a los pacientes y a su equipo de atención una imagen completa de la genética de cada tumor junto con información pronóstica y recomendaciones terapéuticas en un plazo de 48 horas.
Más información:
Sheri Skerget et al., El perfil molecular integral del mieloma múltiple identifica el número de copias refinado y los subtipos de expresión, Genética de la naturaleza (2024). DOI: 10.1038/s41588-024-01853-0
Citación:Un estudio genético de 12 años identifica tipos únicos de mieloma múltiple (20 de agosto de 2024) recuperado el 20 de agosto de 2024 de https://medicalxpress.com/news/2024-08-year-genetic-unique-multiple-myeloma.html
Este documento está sujeto a derechos de autor. Salvo que se haga un uso legítimo con fines de estudio o investigación privados, no se podrá reproducir ninguna parte del mismo sin autorización por escrito. El contenido se ofrece únicamente con fines informativos.