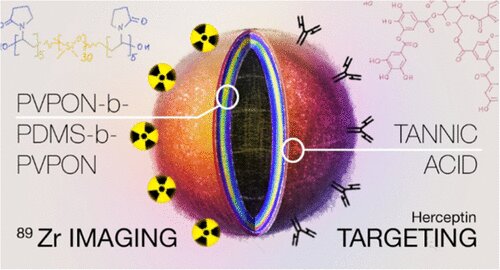
Crédito: Biomacromoléculas (2023). DOI: 10.1021/acs.biomac.2c01539
Una nanovesícula ideal para combatir el cáncer tendría tres funcionalidades: 1) una molécula dirigida con precisión para unirla preferentemente a los marcadores de superficie en las células cancerosas, 2) una señal de radionúclido fuertemente unida que permitiría que una tomografía PET localice las vesículas en el cuerpo, y 3) la capacidad de transportar y liberar un tratamiento farmacológico, como una quimioterapia, en el tumor canceroso.
También cumpliría con otros dos requisitos: tener un método de fabricación simple y fácil, y ser biocompatible y biodegradable en el cuerpo.
Un equipo de la Universidad de Alabama en Birmingham ha descrito ahora un diminuto polimerosoma que, en experimentos preclínicos iniciales, parece superar estos obstáculos. Cada polimerosoma es una esfera hueca con una pared delgada, pero es el revestimiento del polimerosoma lo que marca un paso adelante.
Los polímerosomas de copolímero tribloque de 60 nanómetros tienen ácido tánico degradable, o TA, adsorbido en la superficie a través de enlaces de hidrógeno. Ese TA, a su vez, es capaz de unirse rápida y establemente a una molécula dirigida a anticuerpos monoclonales y un radionúclido de zirconio, o Zr, sin la necesidad de construir enlazadores específicos, como quelantes, dicen Eugenia Kharlampieva, Ph.D., y Suzanne E. Lapi, Ph.D., líderes del equipo de la UAB. Su estudio se publica en la revista Biomacromoléculas.
«En este estudio, hemos desarrollado un enfoque simple para una modificación sin quelantes del PVPON5-PDMS30-PVPON5 nanovesículas de copolímero tribloque, de unos 60 a 80 nanómetros de diámetro, con una capa de polifenol que se puede utilizar simultáneamente para anclar 89radiotrazador Zr u otros iones metálicos activos para imágenes moleculares, y un ligando dirigido a HER2, el anticuerpo monoclonal trastuzumab, para la orientación de nanovesículas a células de cáncer de mama HER2 positivas», dijo Kharlampieva, profesora distinguida en el Departamento de la Facultad de Artes y Ciencias de la UAB de Química.PVPON5 es un bloque de polímero hidrófilo corto de cinco monómeros y PDMS30 es un bloque polimérico hidrofóbico de 30 monómeros más largo dentro del copolímero tribloque.
El cáncer de mama es una de las enfermedades cancerosas más comunes, y las tasas mundiales de mortalidad siguen siendo altas. Los fármacos sistémicos o los anticuerpos terapéuticos son terapias actuales, pero a menudo se asocian con daño y disfunción del corazón. La administración de fármacos guiada por imágenes a un tumor sólido podría permitir una actividad farmacológica eficaz con una toxicidad farmacológica reducida.
«Hasta donde sabemos, nuestro trabajo representa el primer ejemplo de un polimerosoma radiomarcado libre de quelantes capaz de un estudio de imágenes PET de varios días a largo plazo in vivo», dijo Lapi, director de UAB Cyclotron Facility y profesor en el Departamento de Radiología de la UAB. «El enfoque de radiomarcaje desarrollado en este documento puede potencialmente proporcionar una unión estable de un amplio espectro de isótopos sin la lixiviación de radiometales de la membrana de la vesícula in vivo. En particular, este enfoque integra las ventajas inherentes de una membrana de polímero polifenólico con el beneficio de anclar rápidamente las células de cáncer de mama. ligandos dirigidos».
En el estudio, TA en el polímero unido 89Zr4+ radionúclido a través de emparejamiento iónico inespecífico, y el TA también se unió al anticuerpo monoclonal trastuzumab, o Tmab, a través de enlaces de hidrógeno y emparejamiento iónico. Hubo una excelente retención de la 89Zr por hasta siete días, según lo confirmado por tomografías PET en ratones sanos.
«El anclaje no covalente de Tmab a la membrana polimérica puede ser muy ventajoso para la modificación de nanopartículas en comparación con los métodos covalentes desarrollados actualmente, ya que permite una integración fácil y rápida de una amplia gama de proteínas objetivo», dijo Kharlampieva. «Dada la capacidad de estos polimerasomas para encapsular y liberar terapias contra el cáncer, pueden expandirse aún más como portadores terapéuticos dirigidos con precisión para mejorar la salud humana a través de estrategias de administración de fármacos altamente efectivas».
Una hora de incubación de los polimerosomas TA en una solución de 89El oxalato de Zr condujo a rendimientos de radiomarcaje del 97 por ciento, y esos rendimientos se mantuvieron constantes durante uno, tres y siete días. Los polimersomas marcados no fueron citotóxicos cuando se incubaron in vitro con dos líneas de células cancerosas hasta cuatro días. Además, la vinculación de 89Zr a los polimerosomas con Tmab ya unido también tuvo altos rendimientos del 97 por ciento y estabilidad durante siete días. Estos rendimientos de unión son lo suficientemente altos para uso clínico, dicen los investigadores de la UAB.
A continuación, la retención estable de la 89Zr en los polimerosomas TA se demostró indirectamente en ratones.
La biodistribución de libre 89Se ha informado previamente que el radiotrazador Zr se localiza principalmente en la columna vertebral y los fémures de los animales debido a la quelación del zirconio con fracciones de fosfato en el hueso. Los investigadores de la UAB comprobaron que, cuando es libre 89Se inyectó Zr en ratones, casi todo se ubicó en los huesos del fémur después de 24 horas, según lo medido por una tomografía por emisión de positrones (PET). Se observó una biodistribución muy diferente cuando 89Se inyectaron polimerosomas Zr-TA en ratones. Se encontró radiactividad insignificante en los huesos; en cambio, casi toda la radiactividad estaba en el bazo y el hígado. Esa ubicación representa la eliminación esperada conocida de nanovesículas a través del sistema de fagocitos mononucleares para nanomateriales de más de 6 a 8 nanómetros.
«La drástica diferencia observada entre la biodistribución de la libre 89Zr y la vesícula marcada con radiotrazador de metal son importantes, ya que demuestran una capacidad sin obstáculos del nanoportador polimérico para ser rastreado in vivo», dijo Lapi.
El fuerte contraste de imagen en los ratones se retuvo durante siete días, una prueba más de la fuerte retención de la 89Zr en los polimerosomas TA.
La habilidad del 89Se demostró in vitro que los polimerosomas Zr-Tmab-TA se dirigen a las células cancerosas positivas para HER2 mediante la unión diferencial de las nanovesículas a las células de cáncer de mama positivas para HER2 frente a las células negativas para HER2. Los investigadores dicen que se justifican más pruebas para atacar los tumores de cáncer de mama en animales.
Los coprimeros autores del estudio, «Radiomarcaje directo de vesículas de copolímero tribloque dirigidas a trastuzumab con 89Zr para imágenes de tomografía por emisión de positrones», son Veronika Kozlovskaya, Departamento de Química de la UAB, y Maxwell Ducharme, Departamento de Radiología de la UAB.
Otros coautores con Kharlampieva, Lapi, Kozlovskaya y Durcharme son Maksim Dolmat y James M. Omweri, Departamento de Química de la UAB; y Volkan Tekin, Departamento de Radiología de la UAB.
Más información:
Veronika Kozlovskaya et al, Radiomarcado directo de vesículas de copolímero tribloque dirigidas a trastuzumab con 89Zr para imágenes de tomografía por emisión de positrones, Biomacromoléculas (2023). DOI: 10.1021/acs.biomac.2c01539
Citación: Unión fácil y rápida de la molécula de orientación y el radiotrazador al nanoportador de fármacos para la terapia del cáncer (10 de abril de 2023) consultado el 11 de abril de 2023 en https://phys.org/news/2023-04-easy-quick-molecule-radiotracer-drug .html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.