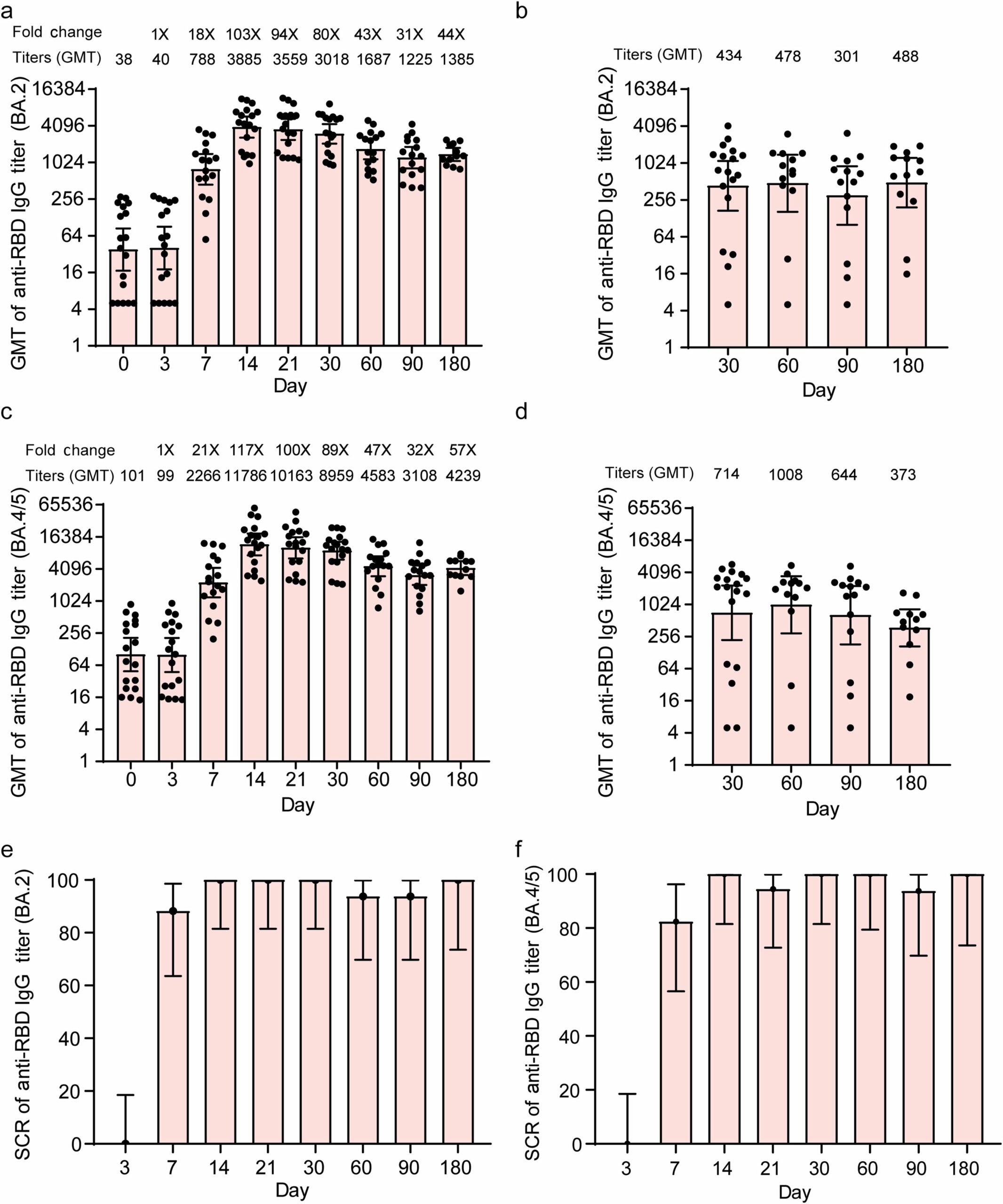
Anticuerpos de unión a RBD contra omicron BA.2 y BA.4/5 de SARS-CoV-2. GMT de títulos de IgG de unión a RBD contra omicron BA.2 en el grupo SYS6006 (a) y el grupo convaleciente (b). GMT de títulos de IgG de unión a RBD contra omicron BA.4/5 en el grupo SYS6006 (c) y el grupo convaleciente (d). SCR de títulos de IgG de unión a RBD frente a omicron BA.2 (e) y omicron BA.4/5 (f). Los datos son GMT (IC del 95 %). Las barras de error indican IC del 95 %. RBD: dominio de unión al receptor de la glicoproteína espiga. Crédito: Metabolismo de la vida (2023). DOI: 10.1093/lifemeta/load019
La pandemia de COVID-19, causada por el síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2), ha resultado en más de 600 millones de casos confirmados y 6,5 millones de muertes en todo el mundo. Las vacunas basadas en ARNm se han convertido en una plataforma líder para la protección contra COVID-19 y se investigan ampliamente en ensayos básicos y clínicos.
SYS6006 (CSPC Pharmaceutical Group) es una vacuna de ARNm COVID-19 en investigación reciente que codifica una secuencia de proteína S de longitud completa de la cepa prototipo SARS-CoV-2 e incorpora las mutaciones clave de las principales variantes epidémicas. En marzo de 2023, fue autorizado para uso emergente en China por la agencia nacional de medicamentos (NMPA) de China. Sin embargo, los datos de los ensayos clínicos aún no se han publicado. Además, se ha propuesto la tercera dosis de vacuna inactivada de COVID-19 como régimen de refuerzo inicial, y vale la pena investigar el segundo refuerzo heterólogo (la cuarta dosis de la vacuna).
Al inscribir sujetos sanos elegibles y pacientes convalecientes de COVID-19, los investigadores del Hospital Central Shanghai Xuhui han trabajado para revelar el primer perfil clínico de seguridad y eficacia de SYS6006. Dieciocho participantes elegibles, que habían completado tres dosis de vacunas COVID-19 inactivadas, recibieron una cuarta dosis de refuerzo de SYS6006-20 μg. Dieciocho pacientes convalecientes de COVID-19 se inscribieron para la recolección de muestras de suero como comparador de inmunogenicidad. Se recopiló e informó la incidencia de eventos adversos dentro de los 30 días posteriores al refuerzo.
Los títulos de anticuerpos anti-RBD de la cepa omicron (BA.2 y BA.4/5) en suero y los títulos de anticuerpos neutralizantes contra pseudovirus de la cepa omicron (BA.2 y BA.4/5) se evaluaron desde el inicio. (día 0) hasta el día 180 posvacunación.
Además, se midieron las respuestas específicas de las células T contra el SARS-CoV-2 mediante la detección de la producción de manchas positivas de interferón gamma (IFN-γ) con el ensayo ELISpot. Este estudio titulado «Seguridad e inmunogenicidad de una vacuna de ARNm de COVID-19 modificada, SYS6006, como refuerzo de cuarta dosis después de tres dosis de vacunas inactivadas en adultos sanos: un ensayo de fase 1 de etiqueta abierta» ahora se publica en la revista. Metabolismo de la vida.
En el estudio, no se informaron eventos adversos graves dentro de los 30 días posteriores a la vacunación. No se informó fiebre de grado 3 ni eventos adversos graves en el grupo SYS6006. En particular, SYS6006 provocó títulos más altos y aumentos más prolongados en anticuerpos anti-RBD y anticuerpos neutralizantes (>90 días) en comparación con el grupo convaleciente (P Estos resultados demostraron que una vacuna de ARNm modificada SYS6006 era segura y altamente inmunogénica como refuerzo heterólogo en pacientes chinos sanos. La fuerte mejora de los títulos de anticuerpos después del refuerzo heterólogo es alentadora, junto con la actividad neutralizante de amplio espectro de estos anticuerpos contra variantes de interés, como omicron BA.2 y BA.4/5. Los títulos en el grupo SYS6006 fueron más altos que los de los pacientes convalecientes.Estos hallazgos sugieren el uso flexible de la vacuna de ARNm como un régimen de refuerzo, lo que podría acelerar el final de la pandemia.
Más información:
Yuzhou Gui et al, Seguridad e inmunogenicidad de una vacuna de ARNm de COVID-19 modificada, SYS6006, como refuerzo de cuarta dosis después de tres dosis de vacunas inactivadas en adultos sanos: un ensayo de fase 1 de etiqueta abierta, Metabolismo de la vida (2023). DOI: 10.1093/lifemeta/load019
Proporcionado por Higher Education Press
Citación: Seguridad e inmunogenicidad de la vacuna de ARNm de COVID-19 SYS6006 evaluada en el ensayo de fase 1 (30 de junio de 2023) consultado el 2 de julio de 2023 en https://medicalxpress.com/news/2023-06-safety-immunogenicity-covid-mrna-vaccine .html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.