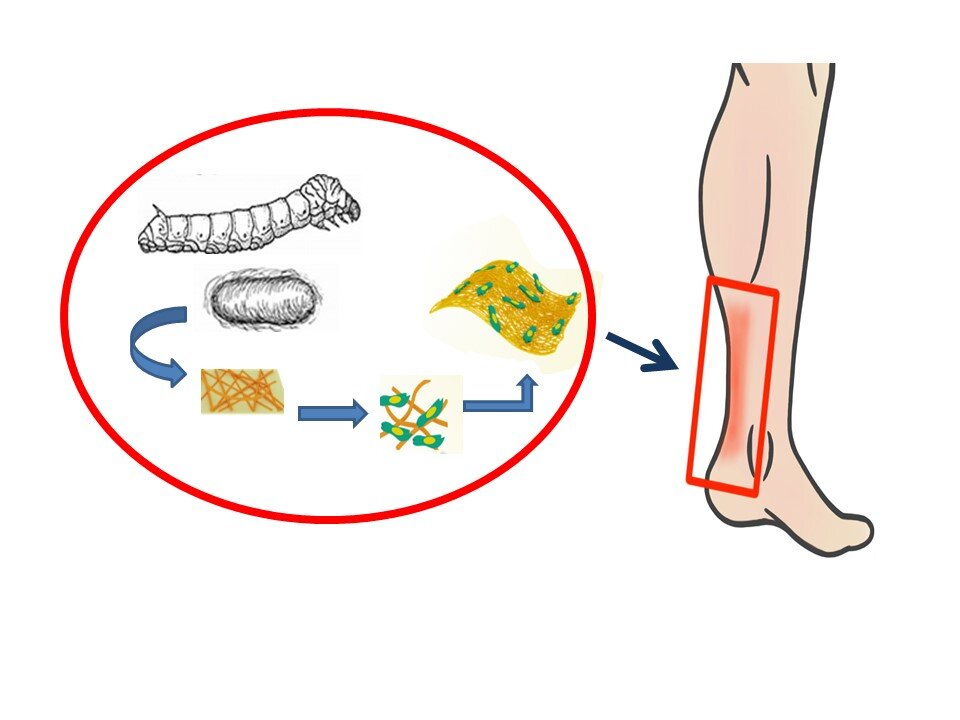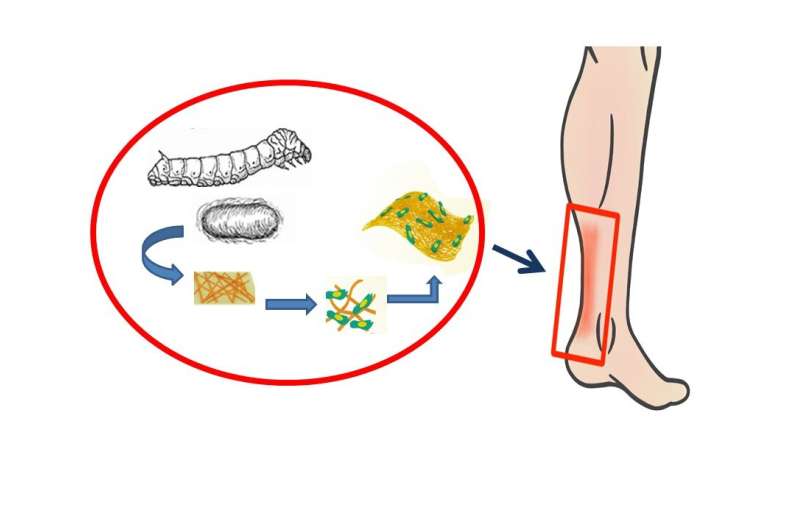
La fibroína de seda de los capullos de gusanos de seda se utiliza en andamios para optimizar los tejidos regenerativos para la reparación de los tendones. Crédito: Instituto Terasaki para la Innovación Biomédica (TIBI)
Solo mencionar un tendón de Aquiles roto haría que cualquiera se estremeciera. Las lesiones de los tendones son bien conocidas por sus procesos de curación prolongados, difíciles y, a menudo, incompletos. El movimiento repentino o repetitivo, experimentado por atletas y trabajadores de fábricas, por ejemplo, aumenta el riesgo de desgarros o rupturas en los tendones; el treinta por ciento de todas las personas tendrán una lesión en el tendón, siendo el riesgo más alto en las mujeres. Además, aquellos que sufren de estas lesiones son más propensos a sufrir más lesiones en el sitio o nunca se recuperan por completo.
Los tendones son bandas de tejido conectivo fibroso que unen los músculos a los huesos. Son tejidos blandos conectados a huesos rígidos; esto crea una interfaz compleja con una estructura muy específica. Después de la lesión, esta estructura se rompe y el tejido conjuntivo cambia de una formación lineal a una torcida. También puede ocurrir una cicatrización excesiva, lo que cambia las propiedades mecánicas del tendón y su capacidad para soportar cargas.
Durante los procesos naturales de curación del cuerpo, se reclutan tendones y otras células para reconstruir la matriz original del tendón de fibras de tejido conectivo alineadas. Pero esta reconstrucción puede llevar semanas o meses y el tendón resultante suele ser imperfecto. Esto resulta en debilidad, dolor crónico y disminución de la calidad de vida.
Los posibles tratamientos para las lesiones de los tendones incluyen injertos de tejido tendinoso de pacientes o donantes, pero estos presentan riesgos como infecciones, rechazo del trasplante o necrosis. Se han intentado trasplantes sintéticos, pero los problemas mecánicos, de biocompatibilidad y de biodegradación han obstaculizado estos esfuerzos.
Otro enfoque consiste en utilizar células madre mesenquimales (MSC), células especializadas que desempeñan un papel fundamental en la regeneración de tejidos. En el sitio de la herida, pueden diferenciarse en varios tipos de células y producir moléculas de señalización que regulan la respuesta inmunitaria, la migración celular y la formación de nuevos vasos sanguíneos; esto permite la regeneración de tejidos.
Sin embargo, los métodos de tratamiento que utilizan la infusión sistémica, la inyección directa o la modificación genética de las CMM presentan sus propias dificultades: la infusión carece de especificidad de orientación al sitio de la lesión, la inyección directa requiere un número de células prohibitivamente alto y la modificación genética es ineficiente y produce células que son difíciles de aislar. .
Otro enfoque más ha sido construir marcos de biomateriales, o andamios, en los que introducir MSC y factores de crecimiento para generar nuevo tejido tendinoso. Un equipo de colaboración del Instituto Terasaki para la Innovación Biomédica (TIBI) ha utilizado este enfoque para desarrollar un método que ha producido mejoras significativas en la regeneración del tendón MSC.
El equipo primero recurrió a la fibroína de seda, una proteína de seda producida por el gusano de seda Bombyx mori. Además de su uso en hermosas telas de seda, la fibroína de seda se usa en dispositivos ópticos y eléctricos, y en varias aplicaciones biomédicas, desde materiales de sutura hasta ligamentos, huesos e incluso tejido corneal creados mediante bioingeniería. Debido a sus cualidades superiores de resistencia, durabilidad, biocompatibilidad y biodegradación, la fibroína de seda es ideal para usar en andamios para tendones.
Con el fin de mejorar la capacidad del andamio para la regeneración de tejidos, el equipo combinó la fibroína de seda con GelMA, un gel de retención de agua a base de gelatina, debido a la biocompatibilidad, la degradación controlable, la rigidez y la capacidad de GelMA para promover la unión y el crecimiento celular.
«Los efectos sinérgicos de la capacidad de GelMA para respaldar la formación de tejido regenerativo y las ventajas estructurales de la fibroína de seda hacen que nuestro material compuesto sea muy adecuado para la reparación de tendones», dijo HanJun Kim, Ph.D., DVM, líder del equipo de TIBI en el proyecto.
Prepararon mezclas con proporciones variables de fibroína de seda y GelMA (SG) y las fabricaron en finas láminas de nanofibras. Luego probaron la estructura de fibra y la elasticidad de las láminas y eligieron una formulación óptima con las mejores propiedades mecánicas. También observaron que la fibroína de seda impartía una mayor porosidad al material; esto mejora la reparación del tendón.
Las hojas SG optimizadas se sembraron con MSC y se sometieron a varias pruebas para medir la compatibilidad y diferenciación de MSC, la producción de factores de crecimiento y la actividad genética que desencadena la formación de matriz.
Las MSC en las láminas SG mostraron un aumento en la viabilidad y proliferación celular en comparación con las láminas de fibroína de seda sin GelMA (SF). El análisis genético mostró que la actividad génica relevante en SG MSC aumentó significativamente, en contraste con las de las hojas SF, que disminuyó.
Las pruebas de tinción revelaron que las MSC en las láminas SG mostraban una tasa de unión de más del 80 % y tenían una forma alargada característica de las células adheridas a una superficie, a diferencia de una tasa de unión del 60 %, con células de forma esférica observadas en SF y GelMA solo superficies.
Pruebas adicionales en un factor de crecimiento secretado por MSC sembradas en láminas de nanofibras mostraron que los factores de crecimiento producidos por las MSC en las láminas SG eran más capaces de reparar el tejido lesionado del tendón cultivado en una placa de cultivo.
También se realizaron experimentos en ratas vivas con tendones de Aquiles lesionados. Se implantaron láminas de nanofibras sembradas con MSC en el sitio de la lesión y las láminas SG promovieron la curación más acelerada, con sitios de lesión reducidos y la formación de fibras tendinosas densamente empaquetadas y bien alineadas y componentes musculares remodelados.
«La remodelación de tejidos para la reparación de tendones es especialmente difícil de lograr», dijo Ali Khademhosseini, Ph.D., Director y CEO de TIBI. «El trabajo realizado aquí avanza significativamente en ese logro».
La investigación fue publicada en Pequeña.
Conectando la ciencia con la medicina: tejido similar a un tendón creado a partir de células madre humanas
Yumeng Xue et al, Hoja de metacriloilo de gelatina y fibroína de seda coelectrohilada sembrada con células madre mesenquimales para la regeneración de tendones, Pequeña (2022). DOI: 10.1002/pequeño.202107714
Proporcionado por el Instituto Terasaki para la Innovación Biomédica
Citación: Reparación de tendones con proteínas de seda (3 de mayo de 2022) recuperado el 3 de mayo de 2022 de https://medicalxpress.com/news/2022-05-tendons-silk-proteins.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.