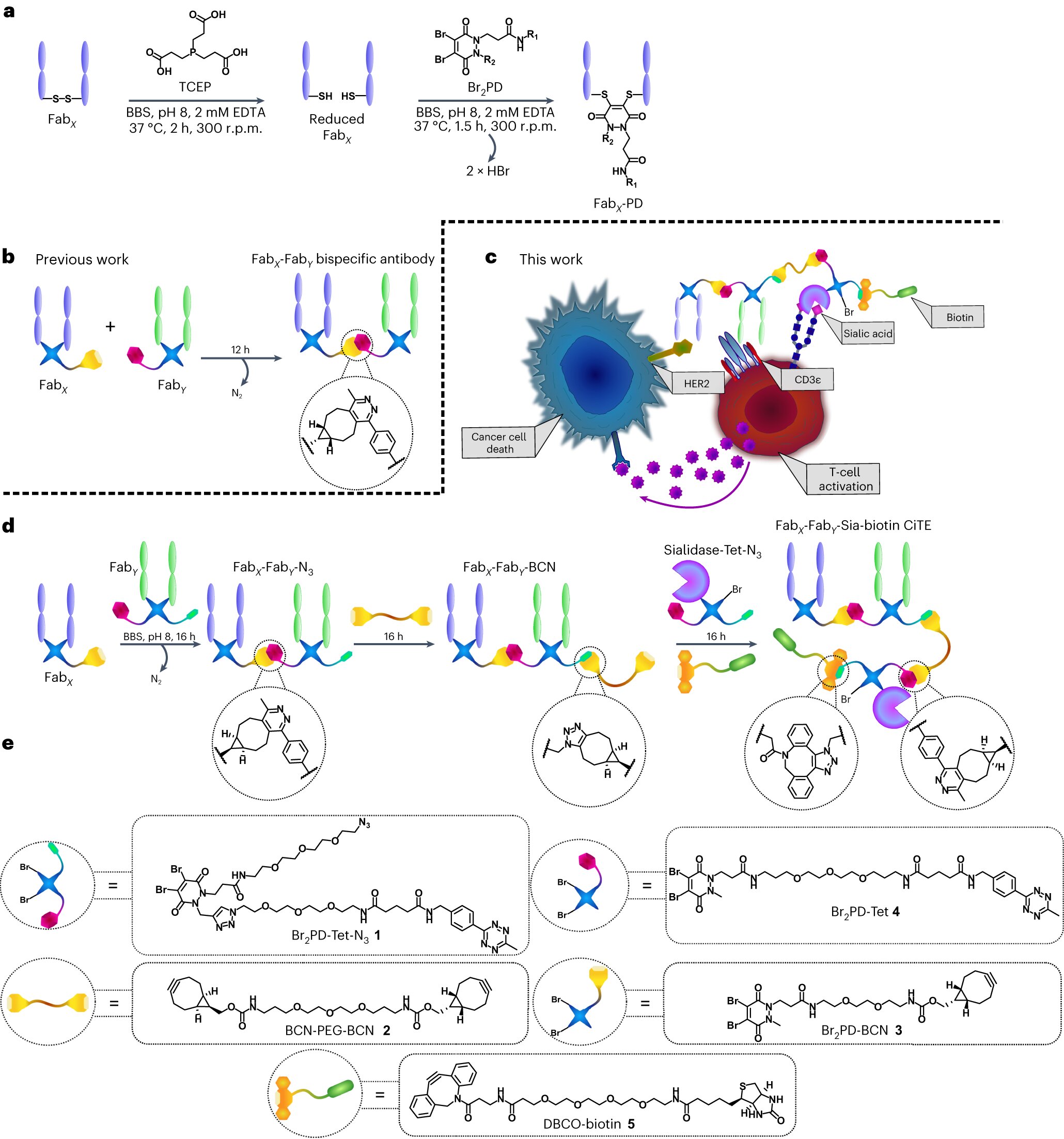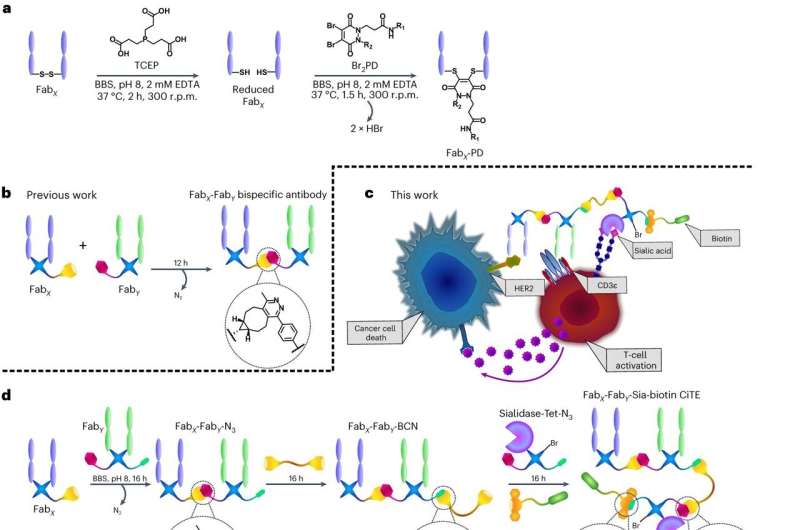
Generación de CiTE y mecanismo biológico subyacente propuesto. a, El método de piridazindiona para la generación de Fabs funcionalizados. El Fab se reduce primero con TCEP para liberar las cisteínas del enlace disulfuro intercatenario único. El Fab reducido luego se hace reaccionar con el Br2PD de elección, a través de un mecanismo de adición-eliminación mediante el cual los tioles desplazan secuencialmente cada átomo de Br para generar un enlace covalente estable entre las cadenas pesada y ligera de la proteína. BBS, solución salina tamponada con borato. bEl método previamente desarrollado para la generación de bsAbs con piridazindionas mediante la química clic SPIEDAC. C, Mecanismo de acción propuesto de un CiTE que contiene sialidasa. El CiTE se une a una célula cancerosa diana a través del compromiso de HER2 ya una célula T a través del correceptor CD3, entrecruzando las dos células. La enzima sialidasa elimina el ácido siálico de las células diana y efectora (T) para mejorar la activación inmunitaria, lo que conduce a una citotoxicidad mediada por células T más potente. El CiTE se funcionaliza con una molécula de biotina para ayudar en la obtención de imágenes o la purificación. dEl método desarrollado en este manuscrito para la generación de construcciones CiTE de tres proteínas funcionalizadas. miLas piridazindionas y otras moléculas pequeñas utilizadas en este trabajo (Br2PD-Tet-N3 1enlazador BCN-PEG-BCN 2hermano2PD–BCN 3hermano2PD–Tet 4 y DBCO-biotina 5) para la biotinilación de las construcciones. Crédito: Química de la naturaleza (2023). DOI: 10.1038/s41557-023-01280-4
Se ha creado una potente terapia contra el cáncer utilizando la «química del clic» ganadora del premio Nobel, donde las moléculas hacen clic entre sí como ladrillos LEGO, en un nuevo estudio realizado por investigadores de la UCL y la Universidad de Stanford.
El estudio, publicado en Química de la naturalezaabre nuevas posibilidades sobre cómo se podrían construir inmunoterapias contra el cáncer de vanguardia en el futuro.
El equipo de investigación creó una terapia contra el cáncer con tres componentes: uno dirigido a la célula cancerosa, otro reclutando un glóbulo blanco llamado célula T para atacar la célula cancerosa y un tercero eliminando parte de las defensas de la célula cancerosa.
Anteriormente, este tipo de terapia de tres componentes solo se había creado utilizando un proceso complejo llamado ingeniería de proteínas, en el que las secuencias de ADN de múltiples proteínas se combinan y se insertan en una sola célula.
Una de las terapias de tres componentes que construyeron los investigadores, que usaba una enzima llamada sialidasa para eliminar los azúcares que la célula cancerosa usa para esconderse, fue especialmente efectiva para matar las células de cáncer de mama en un plato. Los investigadores dijeron que esto demostró que la enzima, que recientemente comenzó a explorarse en la investigación del cáncer, tiene el potencial de ser la base de los agentes anticancerígenos de próxima generación.
El primer autor, el Dr. Peter Szijj (Química de UCL), dijo: «La química de clics es una forma más rápida y más adaptable de construir estos agentes anticancerígenos multifuncionales que la ingeniería de proteínas. Es relativamente fácil adjuntar ‘asas’ de clics a las proteínas para que pueda probar muchas combinaciones rápidamente para probar qué podría funcionar mejor. Usando la ingeniería de proteínas, necesita un mecanismo separado para cada componente».
El autor correspondiente principal, el profesor Vijay Chudasama (Química de la UCL), dijo: «Dado que las proteínas son moléculas grandes y complejas, se requiere una combinación de modificación de proteínas precisa y química de clic confiable para unirlas de manera controlada. Hemos logrado esto y hemos demostrado que nuestra estrategia es una alternativa interesante al uso del enfoque clásico de ingeniería de proteínas».
«Esperamos que mediante el uso de la química para crear agentes anticancerígenos de múltiples proteínas novedosos y altamente sofisticados podamos inspirar a los químicos a cruzar los límites típicos de la disciplina para participar en aplicaciones novedosas en áreas tales como imágenes médicas, diagnósticos y terapias de enfermedades».
La química de clic se basa en dos socios de reacción (mangos de clic) que pueden unirse entre sí de manera muy rápida y selectiva, sin la producción de subproductos tóxicos. Estos controles de clic se pueden agregar a las proteínas, en este caso utilizando piridazindionas (PD) funcionalizadas, lo que permite que las proteínas se unan perfectamente como LEGO.
Los pioneros de la química del clic recibieron el Premio Nobel de Química 2022. La profesora Carolyn R. Bertozzi, de la Universidad de Stanford, coautora de este último artículo, fue una de los tres ganadores del premio por su trabajo sobre química biortogonal: química de clics en células vivas.
Para el nuevo artículo, los investigadores de la UCL primero unieron dos fragmentos de anticuerpos: un fragmento se unía a una célula cancerosa, otro fragmento se unía a una célula T para que destruyera la célula cancerosa. Activadores de células T similares, creados a través de la ingeniería de proteínas, ya han sido aprobados para su uso en humanos y se usan para tratar cánceres como el mieloma múltiple, un cáncer de sangre raro, en los Estados Unidos y Europa.
Luego, el equipo agregó un tercer componente, un inhibidor de puntos de control, que elimina un aspecto de las defensas de una célula cancerosa. Este componente era un fragmento de anticuerpo bloqueador de PD-1, que ya se usa para tratar formas avanzadas específicas de cáncer de piel o de pulmón y reactiva las células inmunitarias para atacar las células cancerosas; o la enzima sialidasa más experimental, que elimina azúcares específicos (ácidos siálicos) en la superficie de la célula cancerosa, así como en la célula T.
Estos azúcares, presentes en todas nuestras células, son producidos en grandes cantidades por las células cancerosas y les ayudan a esconderse de nuestro sistema inmunitario al desactivar las células inmunitarias que se acercan.
El equipo de investigación descubrió que agregar cualquiera de estos componentes mejoraba la eficacia de la terapia para eliminar el cáncer y que agregar sialidasa era especialmente potente.
Los investigadores también agregaron una cuarta molécula, la biotina, lo que les permitió visualizar qué tan bien se unían los componentes a sus respectivos objetivos. Dijeron que esto podría sustituirse por otra molécula pequeña con una función diferente, por ejemplo, para minimizar los efectos secundarios al enmascarar la construcción de la proteína hasta que alcance su objetivo previsto: el cáncer.
En el artículo, los investigadores dijeron que el uso de la química de esta manera para crear terapias contra el cáncer mostró «mucho potencial sin explotar que aún está esperando ser descubierto».
Esta terapia que contiene la enzima sialidasa ahora debe probarse en animales antes de que puedan comenzar los ensayos con humanos.
Más información:
Peter A. Szijj et al, Generación química de activadores de células T inhibitorias de puntos de control para el tratamiento del cáncer, Química de la naturaleza (2023). DOI: 10.1038/s41557-023-01280-4
Citación: Potente terapia anticancerígena creada con ‘química de clic’ (24 de julio de 2023) consultado el 24 de julio de 2023 en https://phys.org/news/2023-07-potent-anti-cancer-therapy-click-chemistry.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.