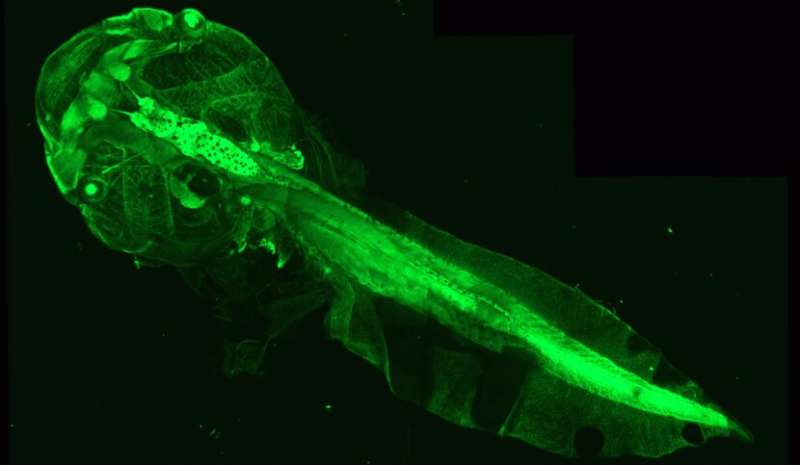
Renacuajo transgénico de Xenopus en el que la sustancia blanca (mielina) aparece por fluorescencia en verde. Crédito: David Akbar y Elodie Martin.
Actualmente no existe ningún tratamiento que pueda detener la progresión silenciosa de la esclerosis múltiple, y muchos medicamentos prometedores han resultado ineficaces en los ensayos clínicos. Para reducir esta tasa de fracaso y predecir mejor el potencial de las moléculas candidatas, investigadores del Paris Brain Institute, coordinados por Bernard Zalc, han desarrollado un nuevo modelo de la enfermedad descrita en Cerebro.
El modelo permite correlacionar la degeneración o regeneración de la mielina con la evolución de las capacidades cognitivas y motoras. Esto pone en el horizonte una mejor orientación de las moléculas que probablemente promuevan la remielinización y detengan el desarrollo de enfermedades.
En la esclerosis múltiple (EM), el sistema inmunitario ataca por error al cerebro y la médula espinal, provocando la pérdida completa de la mielina. “Sintetizada por células especializadas, los oligodendrocitos, la mielina protege las fibras nerviosas, garantiza la buena conducción de los impulsos nerviosos y proporciona nutrientes a los axones”, dice Zalc.
“Esta vaina protectora envuelve las fibras nerviosas y es fundamental para su correcto funcionamiento. Su desaparición, denominada desmielinización, provoca síntomas sensoriales y motores: debilidad de los miembros inferiores o superiores, pérdida del equilibrio, sensibilidad y trastornos de la visión”.
En los últimos 30 años se han realizado importantes avances terapéuticos en el control del componente inflamatorio de la esclerosis múltiple, reduciendo así el daño causado por el sistema inmunitario durante las recaídas de la enfermedad. A pesar de este progreso, todavía hay una progresión de la discapacidad en los pacientes, a pesar de que son tratados con inmunoterapias efectivas. ¿La razón? Neurodegeneración. Esencialmente independiente de la inflamación, justifica la necesidad de tratamientos reparadores.
Sin embargo, reparar las lesiones de la vaina de mielina, o remielinización, es un verdadero desafío. Los fracasos clínicos se han multiplicado a lo largo de los años.
«¿Por qué las moléculas candidatas nos decepcionan sistemáticamente cuando se prueban en humanos? Una posible explicación: en la etapa preclínica, se evalúa su capacidad para generar nuevas células productoras de mielina. Este criterio, basado en la observación de tejidos, no es suficiente. Para el Para que el fármaco sea efectivo, también debe mejorar los síntomas de la enfermedad o incluso restaurar completamente las capacidades sensoriales y motoras, explica el investigador. Pero en la actualidad, es difícil establecer la conexión entre una determinada lesión desmielinizante y un déficit sensoriomotor específico». dice Zalc.
Un puente entre las lesiones y el comportamiento
Para llenar este vacío en la comprensión, los investigadores del equipo de Catherine Lubetzki y Bruno Stankoff en el Paris Brain Institute han imaginado una nueva herramienta. Utilizaron renacuajos de Xenopus genéticamente modificados, un anfibio con un cuerpo perfectamente transparente en esta etapa de desarrollo. Esta característica facilita el recuento de la cantidad de oligodendrocitos productores de mielina dentro del nervio óptico y luego correlaciona este indicador con las habilidades motoras y de comportamiento del animal.
Debido a que los cambios en la cantidad de oligodendrocitos indican un proceso de desmielinización o remielinización, el equipo desarrolló un proceso para inducir estos eventos a pedido: los investigadores introdujeron una sustancia llamada metronidazol en el acuario de renacuajos que, en las condiciones en que se usó, provocó la pérdida de oligodendrocitos en el nervio óptico de los animales. Esta pérdida se correlacionó con la discapacidad visual, evaluada mediante una prueba de evitación de objetivos virtuales.
Después de la exposición al metronidazol, los investigadores observaron la reparación espontánea de la mielina, medida por un aumento en el número de oligodendrocitos y una mejora en los resultados de las pruebas visuales. Luego demostraron que este fenómeno podría acelerarse presentando renacuajos con moléculas que promueven la remielinización.
«Nuestros resultados muestran que la variación en el rendimiento motor y sensorial está perfectamente correlacionada con el nivel de desmielinización y la remielinización de los tejidos. Por lo tanto, este modelo es ideal para probar el potencial de remielinización de nuevos medicamentos antes de lanzar ensayos clínicos largos y costosos», dice Zalc.
Existe una necesidad urgente de encontrar moléculas capaces de actuar sobre la desmielinización que, en su forma crónica, conduce al daño axónico irreversible responsable de la muerte neuronal. La discapacidad entonces progresa inexorablemente.
“Esta nueva herramienta, que permite la monitorización in vivo, tiene el potencial de avanzar en el conocimiento de la relación entre los trastornos visuales, uno de los síntomas más comunes de la esclerosis múltiple, y las lesiones de desmielinización asociadas”, concluye el investigador. «Este es un verdadero trampolín para el futuro éxito terapéutico».
Más información:
Esther Henriet et al, Supervisión de la recuperación después de la desmielinización del SNC, una herramienta novedosa para eliminar el riesgo de las estrategias pro-remielinizantes, Cerebro (2023). DOI: 10.1093/cerebro/awad051
Citación: Nuevo modelo de esclerosis múltiple correlaciona la desmielinización con la evolución de las capacidades cognitivas y motoras (3 de mayo de 2023) consultado el 3 de mayo de 2023 en https://medicalxpress.com/news/2023-05-multiple-sclerosis-demyelination-evolution-cognitive. html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.




