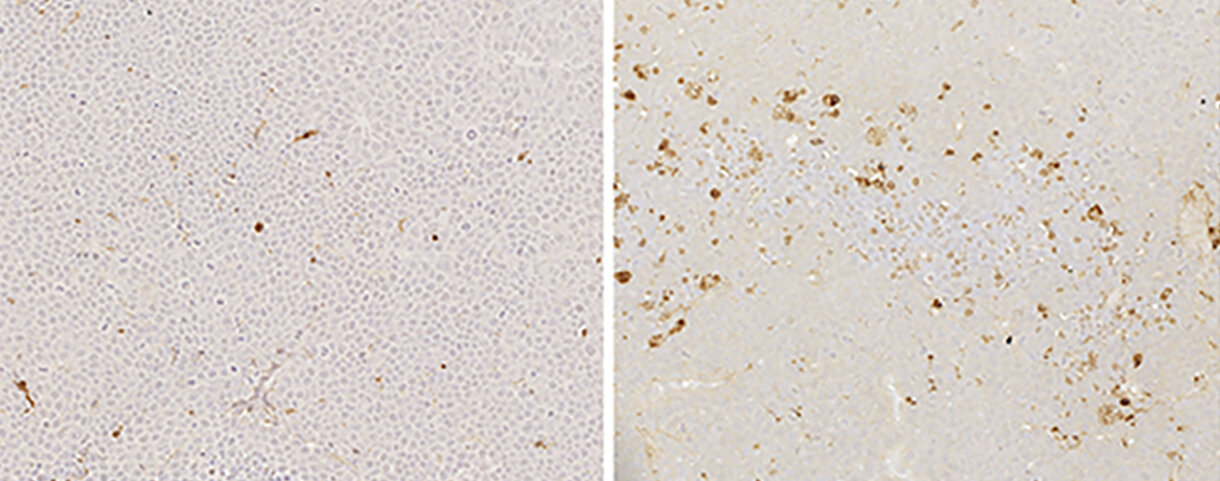
En comparación con un control (izquierda), el tratamiento con un receptor señuelo BCMA soluble (derecha) aumenta la cantidad de células cancerosas que mueren (marrón) en un tumor de mieloma múltiple que crece en ratones. Crédito: © 2022 Miao et al. Publicado originalmente en Revista de Medicina Experimental. 10.1084/jem.20220214
Investigadores de la Universidad de Stanford han desarrollado moléculas de «receptor señuelo» que inhiben el crecimiento tanto del mieloma múltiple (MM) como del linfoma difuso de células B grandes (DLBCL) en ratones. Las moléculas, descritas en un estudio que se publicará el 26 de julio en la Revista de Medicina Experimental (JEM), también se descubrió que no eran tóxicos en los monos, lo que sugiere que podrían usarse para tratar a los humanos con cualquiera de estas enfermedades mortales, que son dos de los cánceres de la sangre más comunes en todo el mundo.
Tanto el MM como el DLBCL son cánceres que se desarrollan a partir de las células B productoras de anticuerpos del cuerpo. La tasa de supervivencia a cinco años para los pacientes diagnosticados con cualquiera de estas enfermedades es inferior al 60 %. En los últimos años, el uso de células CAR T modificadas genéticamente para destruir específicamente las células B cancerosas ha resultado eficaz en algunos pacientes. Sin embargo, este enfoque inmunoterapéutico a menudo tiene efectos secundarios significativos y no es adecuado para pacientes de edad avanzada, en quienes el MM y el DLBCL son particularmente comunes.
«Por lo tanto, aún se necesitan terapias dirigidas seguras y efectivas para los pacientes que agotan las opciones de tratamiento actualmente disponibles», dice la Dra. Yu Rebecca Miao, instructora del Departamento de Oncología Radioterápica de la Universidad de Stanford. Miao dirigió el nuevo estudio con el Dr. Kaushik Thakkar de la Universidad de Stanford y el profesor Amato J. Giaccia, que ahora trabaja en el Instituto Oxford de Oncología Radioterápica de la Universidad de Oxford.
Miao y sus colegas sospecharon que dos proteínas de señalización celular llamadas APRIL y BAFF podrían ser objetivos terapéuticos efectivos para MM y DLBCL. Al unirse a varias proteínas receptoras de la superficie celular diferentes, APRIL y BAFF controlan el desarrollo de las células B normales. Pero los niveles elevados de APRIL y BAFF promueven el crecimiento y la supervivencia de las células B malignas, lo que facilita la progresión del cáncer de sangre y la resistencia al tratamiento. En particular, APRIL está relacionado con la progresión de MM, mientras que BAFF está asociado con DLBCL.
BCMA es un receptor de superficie de células B que se une tanto a APRIL como a BAFF. Miao y sus colegas investigaron si una versión soluble de BCMA, no adherida a la superficie de las células B, actuaría como un «receptor señuelo» para absorber el exceso de APRIL y BAFF y evitar que estas proteínas impulsen el crecimiento de células B cancerosas.
Los investigadores encontraron que el BCMA soluble podía unirse a APRIL e inhibir el crecimiento de MM en ratones. Sin embargo, el receptor señuelo solo se unió débilmente a BAFF y, por lo tanto, no pudo reducir el crecimiento de DLBCL.
Por lo tanto, Miao y sus colegas diseñaron una versión mutante de BCMA soluble que se une fuertemente tanto a APRIL como a BAFF. Esta molécula, denominada sBCMA-Fc V3, pudo impedir el crecimiento de MM y DLBCL en roedores.
En particular, sBCMA-Fc V3 también redujo la actividad de APRIL y BAFF en monos cynomolgus sin causar efectos secundarios significativos. Esto sugiere que el tratamiento con sBCMA-Fc V3 o receptores señuelo similares podría ser seguro y efectivo en humanos.
«En conjunto, nuestros datos respaldan a sBCMA-Fc V3 como un candidato clínicamente viable para el tratamiento de MM y DLBCL», dice Miao. «Las funciones biológicas de BAFF y APRIL no se limitan a las neoplasias malignas de las células B, sino que se extienden a los trastornos autoinmunes y otras enfermedades provocadas por las células B patológicas, lo que sugiere una indicación clínica aún más amplia para sBCMA-Fc V3».
El equipo desarrolla y valida la terapia CAR T tres en uno
Yu Rebecca Miao et al, Revista de Medicina Experimental (2022). DOI: 10.1084/jem.20220214
Citación: Los investigadores usan una molécula personalizada para detener el crecimiento del mieloma múltiple y el linfoma difuso de células B grandes en ratones (26 de julio de 2022) consultado el 26 de julio de 2022 en https://medicalxpress.com/news/2022-07-custom-molecule-halt- crecimiento-multiple.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.