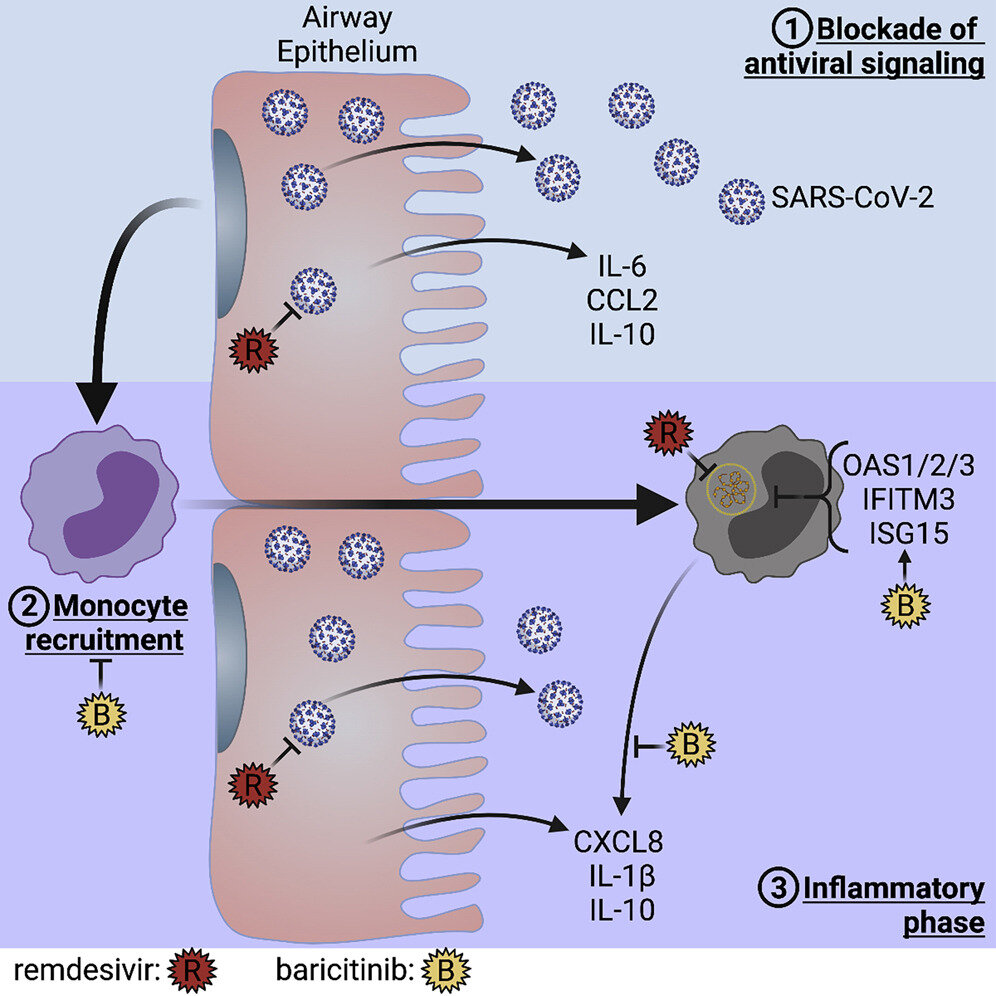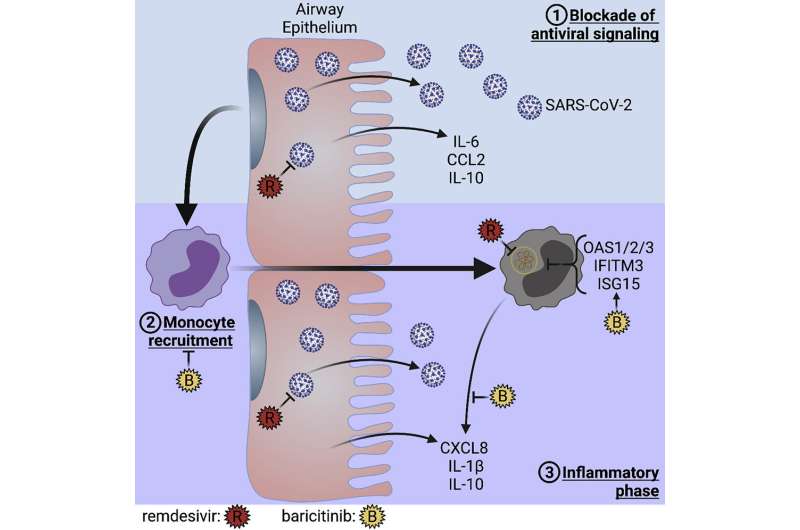
Gráficamente abstracto. Crédito: Informes de celda (2022). DOI: 10.1016/j.celrep.2022.110945
Determinar cómo el SARS-CoV-2, el virus que causa el COVID-19, pasa de una etapa temprana de infección, cuando los pacientes son en gran parte asintomáticos, a una etapa posterior en la que las personas pueden experimentar una inflamación potencialmente mortal en los pulmones, es un paso fundamental en la comprensión de cómo atacar y tratar la enfermedad de manera más eficiente. Pero ese proceso de transición es complejo y no puede estudiarse fácilmente como sucede en el cuerpo humano.
Usando un modelo de laboratorio que adaptaron de un modelo desarrollado previamente para estudiar la fibrosis quística, una enfermedad genética que afecta al pulmón, los investigadores de la Universidad de Emory pudieron replicar esta compleja interacción. Al hacerlo, identificaron el tipo de célula inmunitaria clave que impulsa la transición de la COVID-19 temprana a la tardía y pudieron probar fármacos candidatos en esas células, demostrando su impacto en la eliminación viral y la inflamación.
Los resultados de esta nueva investigación están ahora impresos y en línea como un artículo de acceso abierto en Informes de celda. El estudio concluye que los monocitos que se infiltran en los pulmones (un tipo de célula inmunitaria que puede migrar a los tejidos) impulsan el desarrollo de complicaciones inflamatorias en la COVID-19 y son un objetivo crítico para el tratamiento. Además, el estudio detalla cómo el medicamento antiviral remdesivir y el inmunomodulador baricitinib se pueden usar solos o en combinación para atacar esos monocitos.
«El SARS-CoV-2 realmente altera la forma en que funciona el sistema inmunitario. Los casos graves muestran una respuesta inmunitaria disfuncional y, lamentablemente, no entendemos completamente por qué algunos pacientes son susceptibles a esa respuesta grave y otros no». dice la autora principal Rabindra Tirouvanziam, Ph.D., inmunóloga y profesora asociada en el Departamento de Pediatría de la Facultad de Medicina de la Universidad de Emory. «Nuestro estudio responde a una necesidad insatisfecha al imitar este proceso in vitro y ver cómo se pueden usar los tratamientos para prevenir algunos de los peores efectos de la enfermedad, mejorando así los resultados de los pacientes».
Es importante destacar que el estudio documenta que los datos obtenidos a través del modelo de laboratorio reflejan los datos in vivo recopilados de pacientes hospitalizados con COVID-19. Dado que el proceso de transición es muy difícil de observar en los pacientes, esta investigación proporciona un eslabón de información faltante y una manera de comprender mejor cómo y cuándo los tratamientos con COVID-19 pueden funcionar mejor.
El modelo utilizado en el estudio imita la secuencia de eventos que sucede cuando una persona se infecta con el virus COVID-19. Se basa en el crecimiento de células epiteliales humanas que recubren los pulmones con la parte superior expuesta al aire. Luego, estas células se infectan con SARS-CoV-2 y el modelo permite que los monocitos sanguíneos transmigren a través del epitelio infectado, donde adquieren el virus. Los medicamentos contra la COVID-19 se pueden agregar en cualquier momento para medir cómo afectan la infección y la respuesta inmunitaria en las células epiteliales y los monocitos que se infiltran en los pulmones en diferentes etapas.
En la etapa temprana de la infección por SARS-CoV-2, el virus se replica rápidamente pero evita activamente atraer células inmunitarias de «primera respuesta», llamadas «neutrófilos», que pueden iniciar una inflamación temprana y la eliminación del virus. La persona infectada no desarrolla síntomas y, de hecho, podría replicarse y luego eliminar el virus sin experimentar ningún síntoma. Pero eventualmente, los monocitos también responden; estas células inmunitarias viven más que los neutrófilos y también pueden transmigrar a los pulmones para adquirir el virus y copiar su patrón genético, lo que le indica al cuerpo que intensifique su respuesta inmunitaria. Es precisamente esa escalada la que puede desencadenar un exceso de inflamación.
«La escalada es el problema», dice Tirouvanziam. «Puede que quede poco o ningún virus vivo, pero los monocitos que se infiltran en los pulmones adquirirán y replicarán su secuencia y mantendrán la respuesta inmune, por lo que la inflamación es persistente y puede acumularse rápidamente».
El estudio encontró que el uso combinado de dos tratamientos aprobados por la FDA para COVID-19, remdesivir y baricitinib, mejora la señalización antiviral y la eliminación viral de los monocitos infectados con SARS-CoV-2. Destaca que el momento de los tratamientos terapéuticos es fundamental para evitar la inflamación grave, que puede conducir a la afección potencialmente mortal conocida como síndrome de dificultad respiratoria aguda.
El modelo de vía aérea pequeña en este estudio es único en el sentido de que utiliza células humanas en un sistema que imita el entorno pulmonar. Tirouvanziam dice que esta es una plataforma ideal para probar más medicamentos contra las variantes del SARS-CoV-2. «Es importante tener en cuenta que esto no ha terminado. Constantemente surgen nuevas variantes y, en el futuro previsible, probablemente estaremos expuestos a ellas varias veces al año. Hay una necesidad urgente de seguir desarrollando y probando medicamentos para contrarrestar estas variantes», dice Tirouvanziam.
A la caza de las células inmunitarias que predisponen a las personas a una COVID-19 grave
Brian Dobosh et al, Baricitinib atenúa la fase proinflamatoria de COVID-19 impulsada por monocitos que infiltran los pulmones, Informes de celda (2022). DOI: 10.1016/j.celrep.2022.110945
Citación: Los inmunólogos identifican el objetivo crítico de las células inmunitarias para tratar las complicaciones de la COVID-19 (14 de junio de 2022) consultado el 14 de junio de 2022 en https://medicalxpress.com/news/2022-06-immunologists-critical-immune-cell-covid-.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.