Al estudiar un tipo mortal de cáncer de mama llamado triple negativo, los científicos de Johns Hopkins Medicine dicen que han identificado diferencias moleculares clave entre las células cancerosas que se adhieren a un tumor inicial y aquellas que se aventuran a formar tumores distantes.
La investigación, que utiliza modelos de ratones y tejidos humanos, podría allanar el camino para desarrollar nuevos tratamientos que se dirijan a tales variaciones moleculares.
Un informe sobre los hallazgos se publica el 3 de agosto en Ciencia Medicina Traslacional.
«Hace tiempo que necesitábamos nuevos objetivos y opciones de tratamiento para los cánceres de mama triple negativos», dice Andrew Ewald, Ph.D., profesor de Virginia DeAcetis en Investigación de Ciencias Básicas y Director del Departamento de Biología Celular de la Facultad de Medicina de la Universidad Johns Hopkins y co-líder del Programa de Metástasis e Invasión del Cáncer en el Johns Hopkins Kimmel Cancer Center. «Estos cánceres a menudo regresan dentro de los tres años posteriores al diagnóstico, y los tratamientos utilizados para otros cánceres de mama no suelen funcionar para el triple negativo».
Se estima que entre el 10 % y el 20 % de los 280 000 cánceres de mama diagnosticados en los EE. UU. cada año son triple negativos, y la tasa es más alta entre las mujeres afroamericanas, que tienen el doble de probabilidades que otras de experimentar esta forma de la enfermedad.
El carácter letal de este tipo de cáncer viene marcado por el hecho de que sus células carecen de banderas moleculares en su superficie que conectan con las hormonas estrógeno y progesterona y una proteína promotora del crecimiento del cáncer llamada Her2-neu. Muchas terapias actuales contra el cáncer de mama funcionan al apuntar a esas banderas, lo que las vuelve de poca utilidad para las personas con tumores triple negativos.
Para el estudio actual, el equipo de investigación analizó las diferencias moleculares entre los sitios de cáncer de mama triple negativo iniciales o primarios y las áreas donde se propagó, o sitios metastásicos, entre tres tipos diferentes de células: modelos de ratón, cánceres humanos implantados en ratones y muestras de tejidos primarios y metastásicos tomadas de ocho pacientes tratados en el Hospital Johns Hopkins.
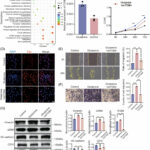
Los investigadores utilizaron una combinación de aprendizaje automático, imágenes celulares y análisis bioquímico para identificar las diferencias en los patrones de expresión genética de los tumores iniciales y metastásicos.
«La mala noticia de nuestro estudio es que las células de los sitios metastásicos están súper optimizadas para la migración y la resistencia al tratamiento», dice Ewald. «La buena noticia es que identificamos varias proteínas llamadas factores de transcripción que estas células requieren para manejar los desafíos de migrar y prosperar en sitios metastásicos, y es posible que podamos diseñar nuevas terapias que se dirijan a estos factores de transcripción».
Más específicamente, Ewald y la becaria postdoctoral de Johns Hopkins, Eloïse Grasset, Ph.D., y otros en el equipo de investigación encontraron varias propiedades únicas en las células de ratones diseñados para tener la versión de ratón de los cánceres de mama triple negativos, y ratones implantados con tumores. de personas con cáncer de mama triple negativo.
Los científicos descubrieron que cuando las células de cáncer de mama triple negativas invaden otros tejidos en su camino hacia otra parte del cuerpo, adquieren dos propiedades celulares: mejor movimiento y supervivencia.
Para hacer esto, las células de cáncer de mama obtienen una proteína de esqueleto celular llamada vimentina, que mejora la capacidad migratoria de las llamadas células mesenquimales, un tipo de célula que se encuentra típicamente en los huesos y la médula ósea que se mueve y produce nuevas células.
Las células de cáncer de mama triple negativas también obtienen ventajas de supervivencia al producir una proteína llamada E-cadherina, que generalmente se encuentra en las células epiteliales que recubren los conductos y las cubiertas de los órganos y se renuevan con frecuencia.
Cuando las células de cáncer de mama triple negativas obtienen tales cualidades migratorias y de supervivencia, los científicos clasifican su estado celular como las llamadas células mesenquimales epiteliales híbridas (EMT).
Para observar más de cerca las moléculas involucradas en los estados EMT híbridos, los científicos buscaron la ayuda de Elana Fertig, Ph.D., directora de división y directora asociada de ciencias cuantitativas y codirectora del Instituto de Convergencia en el Centro de Cáncer Johns Hopkins Kimmel, para rastrear los patrones moleculares de células individuales en ensayos celulares que modelan la invasión fuera del tumor primario y la formación de una colonia en un sitio metastásico.
El equipo computacional de Fertig usó técnicas de aprendizaje automático para encontrar patrones entre la expresión de ARN de cada célula, un primo del ADN involucrado en la producción de proteínas. Los científicos descubrieron que la mayoría de las células metastásicas se transforman en el estado EMT híbrido, más móvil y mejor sobreviviente. Luego, el equipo de Ewald validó estos estados en muestras de ocho pacientes con tumores triple negativos, examinando tanto tumores primarios como tejidos de sitios metastásicos de los mismos pacientes.
A nivel molecular, las células más metastásicas produjeron cinco proteínas llamadas factores de transcripción (Grhl2, Foxc2, Zeb1, Zeb2 y Ovol1) que fomentan la producción de proteínas involucradas en la invasión de células cancerosas o en la formación de colonias.
«Las diferencias moleculares entre los tumores metastásicos y primarios son probablemente la razón por la cual las células tumorales metastásicas son tan resistentes a los tratamientos actuales», dice Ewald.
Su equipo está estudiando formas de bloquear los genes de los factores de transcripción o sus proteínas resultantes para detener el crecimiento del cáncer metastásico, así como también si ocurren los mismos cambios moleculares y celulares en otros cánceres, como los de colon, glándulas suprarrenales, estómago y cánceres pequeños. intestino.
Otros investigadores de Johns Hopkins que contribuyeron al estudio incluyen a Matthew Dunworth, Gaurav Sharma, Melanie Loth, Joseph Tandurella, Ashley Cimino-Mathews, Melissa Gentz, Sydney Bracht y Meagan Haynes.
La investigación fue apoyada por la Fundación para la Investigación del Cáncer de Mama, la Fundación Twisted Pink, Hope Scarves, la Fundación Jayne Koskinas Ted Giovanis, el Fondo Cindy Rosencrans para la Investigación del Cáncer de Mama Triple Negativo y el Instituto Nacional del Cáncer de los Institutos Nacionales de Salud (U01CA217846, U54CA268083, 3P30CA006973, U01CA212007, U01CA253403).