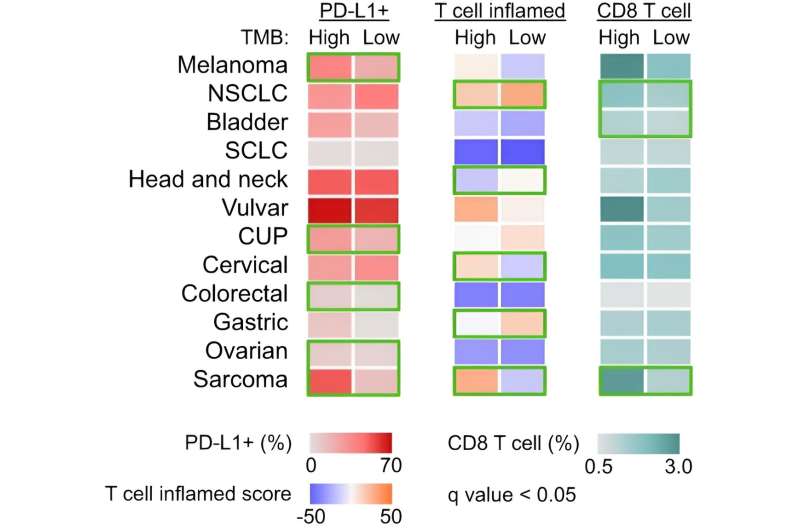
La inmunidad se correlaciona entre los cánceres con TMB alto y bajo utilizando el límite más temprano en el que los ICI son predictivos. La frecuencia de células positivas para PD-L1, la puntuación inflamatoria de células T y la frecuencia de células T CD8+ se comparan entre los cánceres con TMB alto y los cánceres con TMB bajo utilizando el punto de corte más temprano en el que los ICI se asocian con el beneficio de SG. Crédito: Cáncer de la naturaleza (2024). DOI: 10.1038/s43018-024-00752-x
La cantidad de mutaciones en el ADN de los tumores cancerosos puede no ser un indicador de qué tan bien responderán los pacientes a los inhibidores de puntos de control inmunológico (ICI), un tipo de inmunoterapia comúnmente recetado, informó en un estudio retrospectivo un equipo dirigido por investigadores del UT Southwestern Medical Center. .
El recomendacionespublicado en Cáncer de la naturalezatrastorna la sabiduría convencional arraigada desde hace mucho tiempo y podría conducir a formas más efectivas de decidir qué pacientes se beneficiarán más de este tipo de tratamiento.
«Nuestro estudio desafía el paradigma de que la carga mutacional del tumor es un marcador universal de cuán inmunogénico será un cáncer. Los estándares actuales que se basan en esta suposición podrían llevar a un tratamiento insuficiente o excesivo de los pacientes», afirmó el líder del estudio, Dr. David Hsieh, profesor asistente. de Medicina Interna de la División de Hematología y Oncología y miembro del Centro Oncológico Integral Harold C. Simmons de UT Southwestern.
Los ICI han revolucionado la terapia para varios tipos de cáncer desde que la Administración de Alimentos y Medicamentos de EE. UU. aprobó el primer fármaco de esta categoría en 2011. Desde entonces, otros siete ICI se han unido al mercado estadounidense. Todos funcionan bloqueando los puntos de control de proteínas que impiden que el sistema inmunológico ataque las células cancerosas.
Aunque los ICI pueden prolongar significativamente la supervivencia, los ensayos clínicos han demostrado que funcionan sólo en una fracción de pacientes, y se cree que el número de mutaciones presentes en las células cancerosas es un predictor confiable del éxito de los ICI.
Por ejemplo, pembrolizumab, un ICI comúnmente recetado para tratar una variedad de cánceres, incluido el melanoma, el cáncer de pulmón de células no pequeñas y el carcinoma de células renales, está aprobado para pacientes cuyos tumores tienen 10 o más mutaciones por millón de pares de bases de ADN y cuyos cánceres han progresado con los tratamientos estándar.
Sin embargo, dijo el Dr. Hsieh, la idea de que la carga de mutaciones tumorales (TMB, por sus siglas en inglés), o el número de mutaciones presentes en un tumor, es un marcador consistente de qué tan bien funcionarán los ICI podría ser una suposición errónea. Los estudios que formaron la base de esta idea fueron relativamente pequeños e incluyeron un número limitado de tipos de cáncer. Además, dijo, el límite de 10 o más mutaciones utilizado para prescribir pembrolizumab se basó en evidencia débil.
Para determinar cómo se relaciona TMB con los resultados con ICI, el Dr. Hsieh y sus colegas se basaron en una base de datos administrada por Caris Precision Oncology Alliance, un grupo de más de 80 centros oncológicos y centros médicos académicos líderes, incluido UT Southwestern. La base de datos incluye información genética no identificada sobre cientos de miles de tumores malignos derivados de pacientes con muchos tipos diferentes de cáncer.
Los investigadores utilizaron esta base de datos para analizar TMB en 70.698 tumores de 27 tipos diferentes de cáncer. Los datos involucraron a 14.736 pacientes tratados con ICI que se dirigen a una proteína de punto de control inmunológico conocida como PD-1/L1 y 55.962 que nunca recibieron un ICI. Luego, los investigadores compararon TMB con los resultados de los pacientes en ambos grupos.
Los resultados mostraron que TMB predijo el beneficio de ICI en sólo 12 de los 27 tipos de cáncer. Entre esos 12 tipos de cáncer, los umbrales de TMB para los beneficios de ICI eran mucho menos de 10 mutaciones por millón de pares de bases de ADN y variaban ampliamente entre los tipos de cáncer, lo que sugiere que el límite para el uso de pembrolizumab era arbitrario.
En algunos tipos de cáncer examinados en el estudio, la TMB se asoció con una mejor supervivencia en los pacientes que nunca recibieron un ICI. En otros, la supervivencia fue peor, lo que sugiere que la carga de mutaciones puede tener efectos independientes en el pronóstico de los pacientes, independientemente de si recibieron inmunoterapia.
Dado que se pensaba que la TMB estimulaba la actividad inmunitaria, explicó el Dr. Hsieh, los médicos a menudo han utilizado factores inmunitarios (como si un tumor tenía un número relativamente alto de células inmunitarias infiltrantes o producía más PD-1/L1) como sustitutos de la TMB.
Para determinar si estas suposiciones eran exactas, los investigadores compararon TMB con información de la base de datos Caris de biopsias de tumores. Si bien algunos tumores con TMB altos tenían características que sugerían una mayor actividad inmune, otros no, lo que sugiere que estas características no eran indicadores confiables.
El Dr. Hsieh dijo que estos hallazgos mostraron que la TMB no es un indicador confiable de si las ICI mejorarán los resultados, un posible cambio de paradigma para este campo. Se necesita más investigación, añadió, para mejorar los resultados de los pacientes con cáncer con ICI.
Más información:
Maishara Muquith et al, Umbrales de carga de mutaciones específicos de tejido asociados con el beneficio y el pronóstico de la terapia anti-PD-1/L1 en cánceres estables en microsatélites, Cáncer de la naturaleza (2024). DOI: 10.1038/s43018-024-00752-x
Citación: Las mutaciones tumorales pueden no predecir la respuesta a la inmunoterapia, según un estudio (2024, 23 de mayo) recuperado el 23 de mayo de 2024 de https://medicalxpress.com/news/2024-05-tumor-mutations-response-immunotherapy.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.






