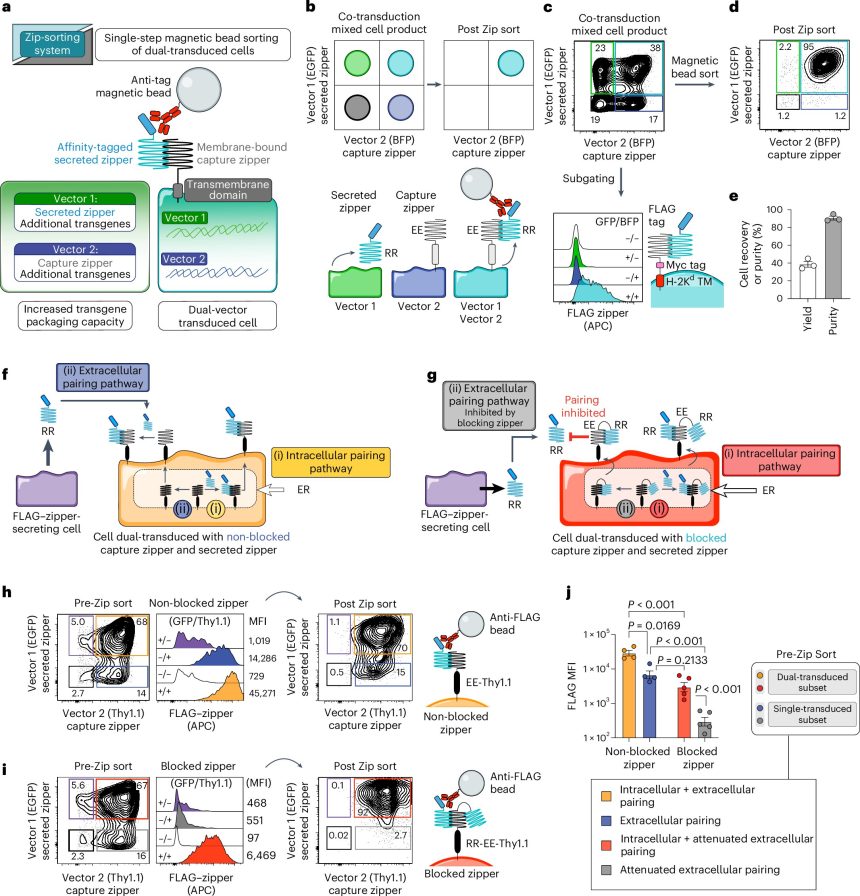
Ingeniería de un sistema de clasificación de células basado en cremalleras de leucina. Crédito: Ingeniería Biomédica de la Naturaleza (2024). DOI: 10.1038/s41551-024-01287-3
Los médicos investigadores de City of Hope han desarrollado una forma de agregar características a las células T para ayudarlas a superar los mecanismos de resistencia a la terapia de células T con receptor de antígeno quimérico (CAR). Su nuevo sistema se describe en un artículo publicado en Ingeniería Biomédica de la Naturaleza.
La terapia con células T con CAR ha revolucionado la atención del cáncer y ofrece una opción poderosa para algunos cánceres de la sangre. Sin embargo, ningún tratamiento es perfecto y algunos pacientes desarrollan resistencia a las terapias con células T con CAR.
«Históricamente, en este campo, las personas han intentado superar las estrategias individuales que los tumores utilizan para evadir las inmunoterapias. Diseñar células T para resistir múltiples estrategias ha sido un desafío debido a la capacidad limitada de empaquetado del ADN de los sistemas de vectores actuales», dijo Scott E. James, MD, Ph.D., profesor clínico asistente en el Departamento de Hematología y Trasplante de Células Hematopoyéticas de City of Hope y autor principal del artículo. «Desarrollamos un nuevo método para facilitar la codificación de numerosas características en las células T con el objetivo de superar múltiples mecanismos de escape de tumores al mismo tiempo».
La terapia con células T con CAR actualmente aprobada toma células inmunitarias del torrente sanguíneo de un paciente y las reprograma para producir un CAR que reconoce y se une a una proteína o antígeno específico que se encuentra en las células cancerosas. Luego, las células T modificadas se reintroducen en el sistema del paciente, donde destruyen las células tumorales específicas a las que ahora se unen. Sin embargo, pueden surgir problemas, incluida una baja expresión del antígeno objetivo que dificulta que las células T lo «vean».
«El tumor esencialmente se vuelve invisible para las células T», explicó el Dr. James. «Una solución ha sido buscar múltiples antígenos o moléculas diferentes al mismo tiempo. Generalmente, la mayoría de los enfoques han implicado apuntar a dos antígenos, pero pudimos apuntar a hasta cuatro usando nuestra nueva estrategia en este proyecto».
Pero no es fácil simplemente agregar varios CAR a una célula T.
El Dr. James compara el problema con quedarse sin capacidad de almacenamiento en su computadora. Al utilizar una unidad zip o flash (o, en este caso, un sistema o vector de entrega de genes adicional), se duplica la capacidad de almacenamiento.
«Existen limitaciones en la cantidad de información genética que podemos introducir en una célula, basándose en el uso de un enfoque de vector único», dijo. «Al utilizar dos vectores y purificar selectivamente las células que recibieron ambos vectores, podemos duplicar la cantidad de espacio disponible para codificar nuevos programas celulares».
Trabajando con colaboradores del Memorial Sloan Kettering Cancer Center, Weill Cornell Medical College, la Universidad de Pennsylvania y los Institutos Nacionales de Salud, el Dr. James y Marcel van den Brink, MD, Ph.D., presidente de City of Hope Los Angeles y National Medical Center y director médico ejecutivo, diseñaron un sistema que utiliza un enfoque de vector dual para duplicar la capacidad de información genética, lo que permite la orientación simultánea de múltiples antígenos.
También permite el uso de receptores de conmutación, que convierten las señales negativas de una célula cancerosa en señales positivas, para reducir el agotamiento de las células T, otro mecanismo de escape del tumor. El enfoque se ha probado con hasta cuatro antígenos y tres receptores de conmutación, mostrando una actividad antitumoral mejorada y células T que proliferaron más y vivieron más tiempo. El sistema, denominado «zip-sorting» por los investigadores, proporciona una poderosa metodología para construir y comparar nuevas terapias celulares.
«Construimos esta plataforma para que los investigadores puedan ahora entregar el doble de información genética a una célula T», dijo el Dr. James. «Para demostrar la utilidad de este sistema, diseñamos células T con múltiples receptores para permitirles responder a múltiples moléculas objetivo y resistir la supresión inmune por parte de las células tumorales».
Si bien el trabajo hasta ahora se ha realizado en modelos de ratón, la esperanza es optimizar la clasificación zip para investigar el método en células humanas. Por ejemplo, el equipo de investigadores está trabajando en un proyecto para probar una gran cantidad de receptores de conmutación para ver qué combinaciones funcionan mejor.
«Nuestros experimentos de prueba de principio demuestran que las células T pueden diseñarse para superar múltiples mecanismos de resistencia tumoral simultáneamente y esto es muy prometedor para la traducción clínica», afirmó el Dr. van den Brink, autor principal del estudio.
Además de utilizar la clasificación zip para agregar CAR y cambiar receptores, la técnica podría tener otras aplicaciones, como potencialmente agregar factores de transcripción, que pueden hacer que las células T proliferen mejor, o interruptores de seguridad que pueden agotar las células T si se vuelven demasiado activas, dijo el Dr. .
«Fue sorprendente que pudiéramos poner tantas características en una célula T y aún así mantener su actividad en un microambiente tumoral que normalmente sería supresor», dijo el Dr. James.
«Ahora podemos diseñar células que sean capaces de evitar múltiples estrategias de evasión inmune, y anteriormente esto había sido un desafío importante para diseñar resistencia a todas estas estrategias a la vez, juntas, en la misma célula. Espero ver qué más podemos hacer. podremos agregar para mejorar aún más la eficacia a largo plazo de las terapias con células T con CAR».
Más información:
Scott E. James et al, Purificación inmunomagnética basada en cremallera de leucina de células T CAR que muestran múltiples receptores, Ingeniería Biomédica de la Naturaleza (2024). DOI: 10.1038/s41551-024-01287-3
Citación: Las células T diseñadas podrían ayudar a los pacientes a superar la resistencia a la terapia con células T con CAR (2024, 24 de diciembre) obtenido el 24 de diciembre de 2024 de https://medicalxpress.com/news/2024-12-cells-patients-resistance-car-cell.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.