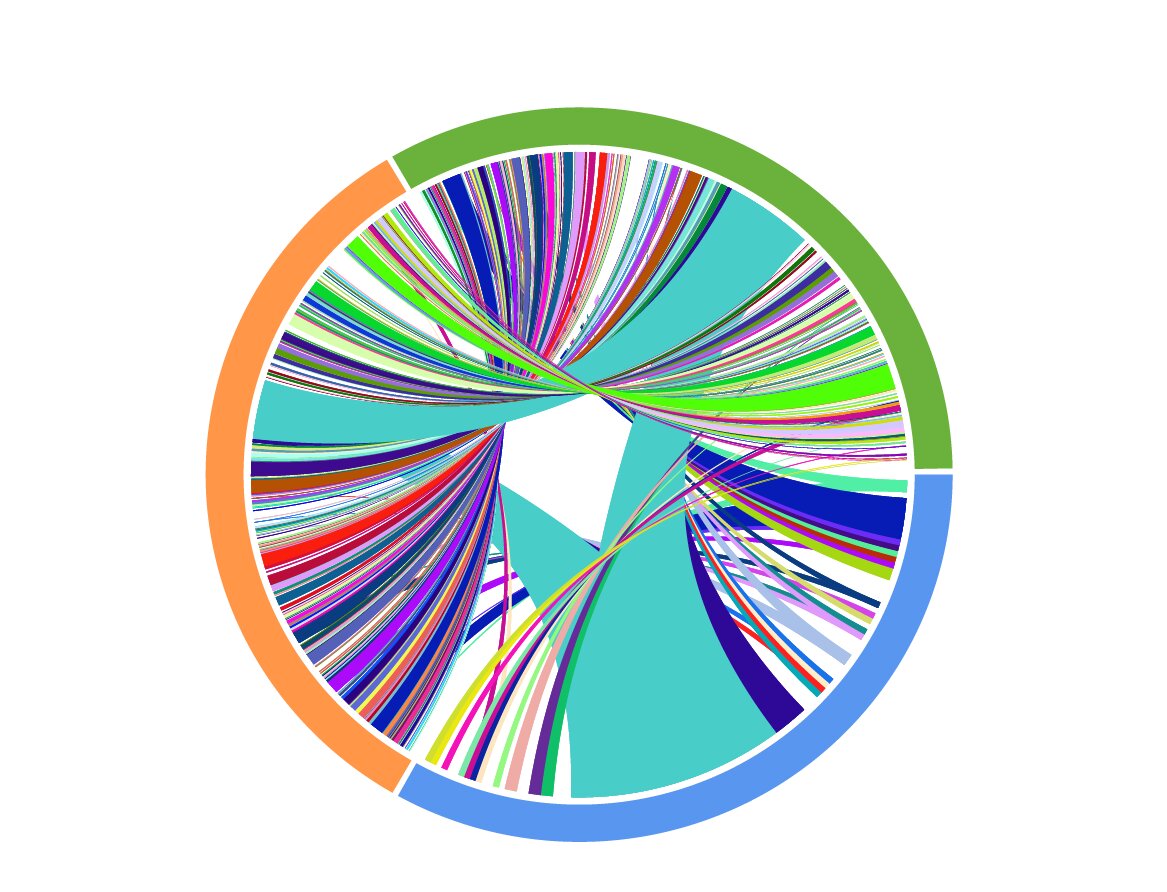
Un diagrama de Circos que representa los resultados de la secuenciación del receptor de células T coincidentes recopilados en un paciente que se somete a una terapia anti-PD1. Los colores indican el momento de la recolección (azul: tratamiento previo, naranja: en tratamiento, verde: más tarde) y las conexiones indican superposición de TCR idénticos. Estos resultados demuestran una sorprendente diversificación de los clonotipos de células T a lo largo del tiempo. Crédito: Yiping Wang/CUIMC
Investigadores de Columbia Engineering y del Centro Médico Irving de la Universidad de Columbia han inventado un nuevo método de secuenciación de ARN que logra resultados de alta calidad a partir de pequeños volúmenes de muestras de tumores congelados. Demostraron el éxito de su técnica en dos estudios clínicos que perfilaron docenas de muestras de tumores, tanto las archivadas como las recién recolectadas, para comprender cómo responden a la terapia antitumoral. El artículo fue publicado el 9 de enero de 2023 por Genética de la Naturaleza.
El uso de la secuenciación de ARN para medir la expresión génica en la resolución de células individuales ha sido una de las herramientas más transformadoras para estudiar tejidos cancerosos durante la última década. Al examinar el ARN de células individuales, los investigadores pueden comprender mejor la diversidad de células dentro de un tumor, así como también cómo estas células tumorales crecen e interactúan con las células inmunitarias. Estos son factores importantes para comprender las características de la progresión del cáncer y la resistencia del cáncer a la terapia, ambos clave para el desarrollo de nuevos tratamientos contra el cáncer.
Una barrera importante para la adopción generalizada de la secuenciación de ARN de una sola célula en los flujos de trabajo clínicos tradicionales ha sido el volumen de tejido fresco requerido, sustancialmente más de lo que se recolecta de forma rutinaria para fines clínicos. Y la necesidad de tejido fresco significa que las muestras deben analizarse inmediatamente una vez que se recolectan. Estos requisitos han limitado significativamente los análisis científicos que se pueden realizar en muestras de pacientes.
Nueva técnica exitosa
Centrado en superar estas barreras, el equipo de Columbia creó un nuevo método de secuenciación que brindó los mejores resultados a partir de una pequeña cantidad de muestras de tumores congelados. Por lo general, recolectados durante los ensayos clínicos y almacenados en biobancos, estos especímenes pueden incluir tejidos de cánceres raros y pacientes con antecedentes o factores de riesgo únicos. La capacidad de la nueva técnica para secuenciar este tipo de muestras aumenta considerablemente el número y la variedad de muestras de tumores disponibles para el análisis científico.
«Estamos muy entusiasmados con este trabajo y su potencial», dijo Elham Azizi, profesor asistente de ingeniería biomédica y profesor asistente Herbert and Florence Irving de investigación de datos sobre el cáncer en el Irving Institute for Cancer Dynamics, quien cosupervisó este estudio con Benjamin Izar. , profesor asistente de medicina en el Centro Oncológico Integral Herbert Irving.
«La capacidad de trabajar con muestras congeladas abre la puerta a colaboraciones multiinstitucionales que impulsarán el descubrimiento de biomarcadores y dianas farmacológicas. También nos brinda la oportunidad de aplicar técnicas computacionales de vanguardia en el análisis y la integración de los datos clínicos desbloqueados. «, explicó Azizi.
Izar agregó: «Y debido a que nuestro método requiere solo una pequeña cantidad de tejido, el resto de la muestra se puede usar para estudios adicionales. Esto realmente es beneficioso para los investigadores, los médicos y, lo que es más importante, para nuestros pacientes».
Los resultados del estudio amplían la comprensión de la progresión del cáncer
El nuevo estudio dirigido por Yiping Wang, Joy Fan y Johannes Melms, aprendices en los laboratorios Izar y Azizi, generó resultados de la secuenciación de ARN de una sola célula, la secuenciación del receptor de células T de una sola célula, la secuenciación del genoma completo y la secuenciación espacial del ARN. (un método innovador de secuenciación de ARN que conserva la arquitectura del tumor in situ), todo realizado en las mismas muestras.
Con la capacidad de unir múltiples modalidades de datos sobre el cáncer, los investigadores proporcionaron una visión integral de las alteraciones genéticas, las funciones celulares, la dinámica de las células inmunitarias y la localización espacial de las células en el contexto del tejido del paciente. Estas mejoras ampliaron significativamente su comprensión de la progresión del cáncer y los mecanismos de resistencia.
El equipo ahora está aplicando sus novedosas técnicas experimentales y computacionales para analizar cohortes clínicas más grandes. Los datos les permiten estudiar mejor la progresión de la enfermedad y examinar el impacto de las terapias en ensayos clínicos en melanoma y otros tipos de cáncer.
ECHIDNA, una nueva herramienta computacional
Paralelamente, los investigadores también están desarrollando una herramienta informática innovadora para el análisis integrador sistemático de los datos del genoma completo y la secuenciación del ARN unicelular, denominada ECHIDNA. Esperan que este algoritmo de aprendizaje automático sea clave para comprender la relación entre las alteraciones genéticas (genotipo) y la función celular (fenotipo) en las células tumorales y lo aplicarán a una cohorte más grande de pacientes con melanoma para caracterizar diversos mecanismos de resistencia al tratamiento. El trabajo futuro también incluirá la construcción de nuevos métodos computacionales para integrar estos datos dentro del contexto espacial del corte histológico para caracterizar la dinámica espacial de las interacciones tumor-célula inmune.
Izar señaló: «Además de comprender el tejido canceroso, nuestro método también permite estudiar la respuesta tisular y la inmunología tisular en otras enfermedades. En el pasado, usamos una versión anterior del método presentado aquí para estudiar la respuesta tisular a la infección letal por COVID-19. a través de múltiples órganos. Esto demuestra un ejemplo de desarrollos que se originan en la investigación del cáncer que pueden impulsar la investigación en ciencias de la vida en general».
Más información:
Yiping Wang et al, Secuenciación multimodal de una sola célula y del genoma completo de muestras clínicas congeladas pequeñas, Genética de la Naturaleza (2023). DOI: 10.1038/s41588-022-01268-9
Citación: La secuenciación multimodal logra resultados de alta calidad a partir de pequeños volúmenes de muestras de tumores congelados (18 de enero de 2023) consultado el 18 de enero de 2023 en https://medicalxpress.com/news/2023-01-multimodal-sequencing-high-quality-results- pequeño.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.