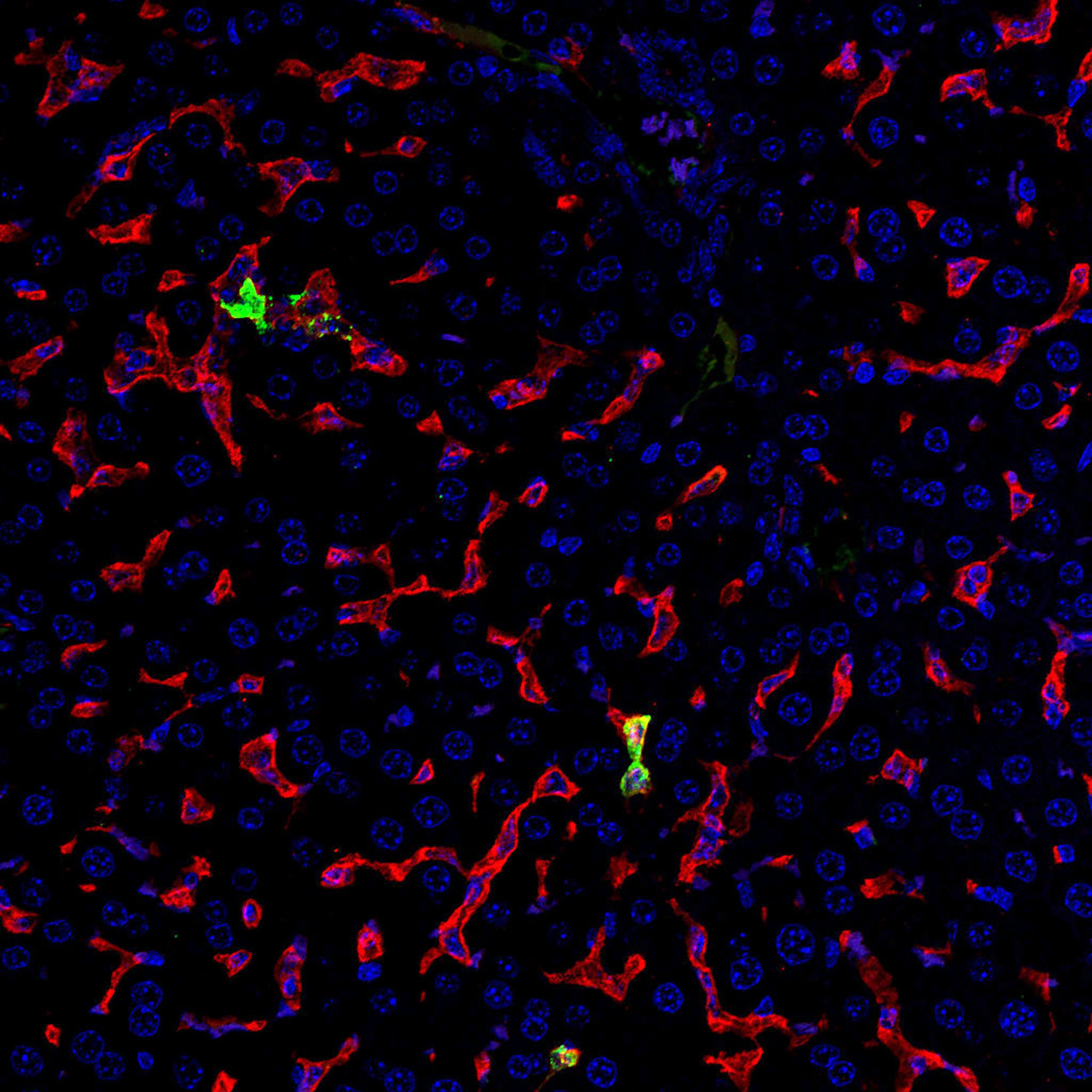
El virus de la fiebre hemorrágica de Crimea-Congo causa una destrucción catastrófica de las células de Kupffer en ratones que carecen de señalización de interferón tipo I, como lo indica una pérdida casi completa del marcador de superficie celular de Kupffer CLEC4F. Por el contrario, esta imagen muestra que las células de Kupffer positivas para CLEC4F (rojas) no se pierden durante la infección en ratones que carecen de la proteína de señalización antiviral mitocondrial donde la actividad del interferón tipo I también fue bloqueada por el anticuerpo. Además, la proteína viral (verde) solo se detectó en las células de Kupffer positivas para CLEC4F (rojas). Los núcleos celulares se tiñeron con azul fluorescente. Estos datos demuestran que la lesión hepática por el virus de la fiebre hemorrágica de Crimea-Congo en ratones deficientes en MAVS es mucho más limitada en comparación con la infección en ratones de tipo salvaje no transgénicos. Crédito: Jeffrey M. Smith, USAMRIID
Los científicos del ejército determinaron que la propia respuesta inmunitaria natural del cuerpo contribuye a la gravedad de la enfermedad en ratones infectados con el virus de la fiebre hemorrágica de Crimea-Congo (CCHFV), que causa una infección viral transmitida por garrapatas generalizada en humanos. Su trabajo, publicado el 19 de mayo de 2022 en Patógenos PLoSproporciona una comprensión más profunda de cómo el virus causa la enfermedad y forma una base para el desarrollo de contramedidas médicas para prevenir y tratar la infección.
El CCHFV es endémico en Asia, África y Europa del Este, y se han producido brotes recientes en Europa Occidental. Por estas razones, es considerado un patógeno prioritario por la Organización Mundial de la Salud. Actualmente no existen medicamentos o vacunas aprobadas contra el CCHFV, que causa enfermedades que van desde mínimamente sintomáticas hasta catastróficas y letales. Si bien no está claro por qué algunos pacientes desarrollan una enfermedad leve y otros sucumben a la enfermedad, los estudios epidemiológicos sugieren que la respuesta inflamatoria del huésped, una reacción compleja del cuerpo que se desencadena cuando el virus invade los tejidos sanos, puede ser un factor importante en mediando el resultado de la enfermedad. Sin embargo, hasta ahora, no se ha demostrado experimentalmente la importancia de la respuesta del huésped para impulsar el proceso de la enfermedad.
Para investigar esta vía, Joseph W. Golden, Ph.D. y sus colegas del Instituto de Investigación Médica de Enfermedades Infecciosas del Ejército de EE. UU. (USAMRIID) demostraron por primera vez que los ratones sin «maquinaria» de detección viral crítica eran menos sensibles a la infección por CCHFV. Estos ratones carecían de una proteína necesaria llamada proteína de señalización antiviral mitocondrial (MAVS) y el hallazgo se produjo incluso cuando el interferón tipo I, otro componente clave de la respuesta inmunitaria, también estaba inactivado. Este fue un hallazgo sorprendente, según Golden, quien dijo que los ratones deberían haber sido hipersensibles a la infección porque carecían de importantes sistemas de protección innatos.
«De hecho, en los ratones con deficiencia de MAVS, el virus no logró inducir una respuesta inflamatoria potente, y los niveles del virus incluso disminuyeron en el hígado, un tejido objetivo clave para este virus», explicó. Esto llevó a los investigadores de USAMRIID a sospechar que la sobreproducción de citoquinas inflamatorias, un tipo de molécula de señalización involucrada en la respuesta inmune, podría estar contribuyendo a la progresión de la enfermedad.
Al estudiar la infección en ratones que carecían de vías clave de citoquinas, los investigadores determinaron que la señalización del receptor TNF-α era un factor importante de la enfermedad mediada por CCHFV. Pudieron proteger a los ratones infectados con CCHFV utilizando anticuerpos dirigidos contra el TNF-α. Sorprendentemente, también determinaron que, si bien una cepa menos virulenta de CCHFV causó una respuesta inflamatoria más leve que una cepa letal del virus, las dos cepas causaron niveles similares de daño hepático. Es importante destacar que su trabajo demuestra que las respuestas inflamatorias ayudan a impulsar los resultados de la enfermedad CCHFV.
USAMRIID ha estudiado CCHFV durante décadas, y con el desarrollo relativamente reciente de sistemas de modelos animales adecuados, Golden y su equipo han centrado su investigación en dos áreas: comprender cómo el virus causa la enfermedad y desarrollar vacunas y medicamentos para prevenir o tratar la infección. El grupo identificó previamente una proteína crítica llamada glicoproteína 38 (GP38) como un importante objetivo de anticuerpos antivirales. Esa investigación allanó el camino para el desarrollo de inmunoterapias que podrían usarse para proteger a los humanos expuestos al virus. También desarrollaron una vacuna de ADN capaz de proteger contra el virus que actualmente se encuentra en desarrollo preclínico. Con este último estudio, el equipo de USAMRIID ha identificado la respuesta inflamatoria del huésped como un nuevo objetivo para la intervención farmacológica.
Su cuerpo de trabajo ofrece la perspectiva de un enfoque terapéutico combinado que se dirige al virus y modula la respuesta del huésped para ayudar a prevenir enfermedades graves, según la coautora del estudio, Aura Garrison, Ph.D. «Con estos avances recientes, esperamos ver pronto el desarrollo de vacunas y terapias para uso humano para mitigar la amenaza del CCHFV», dijo.
Los científicos desarrollan una nueva terapia para el virus de la fiebre hemorrágica de Crimea-Congo
Joseph W. Golden et al, La respuesta inflamatoria del huésped contribuye a la gravedad de la enfermedad en ratones infectados con el virus de la fiebre hemorrágica de Crimea-Congo, Patógenos PLOS (2022). DOI: 10.1371/journal.ppat.1010485
Proporcionado por el Instituto de Investigación Médica de Enfermedades Infecciosas del Ejército de EE. UU.
Citación: La investigación arroja luz sobre el proceso de la enfermedad de la fiebre hemorrágica de Crimea-Congo (20 de mayo de 2022) recuperado el 20 de mayo de 2022 de https://medicalxpress.com/news/2022-05-crimean-congo-hemorrhagic-fever-disease.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.