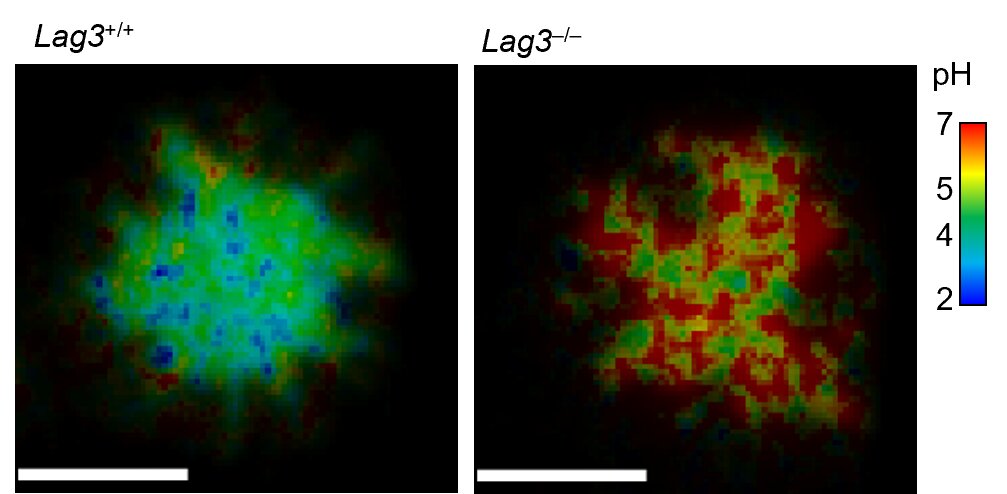
En ratones que expresan LAG3 (imagen de la izquierda), la acumulación de LAG3 en la sinapsis inmunológica en las células T reduce el pH, lo que hace que las condiciones sean más ácidas (verde y azul) en comparación con las condiciones menos ácidas (rojas) en las células T de ratones que no expresan LAG3 (imagen derecha). Crédito: Guy, C. et al. Inmunología de la naturaleza (2022)
La lucha contra el cáncer y las enfermedades crónicas es un trabajo agotador para el sistema inmunológico. Cuando las células T se involucran en este tipo de batalla prolongada, pueden agotarse o ser incapaces de funcionar correctamente. Los reguladores federales aprobaron recientemente una inmunoterapia que revitaliza estas células al bloquear una proteína de punto de control inmunitario llamada LAG3. Pero exactamente cómo funciona LAG3 sigue siendo un misterio, hasta ahora.
Publicado hoy en Inmunología de la naturalezaun nuevo estudio señala cómo LAG3 modula la actividad de las células T, proporcionando información importante para el desarrollo de otras terapias de bloqueo de LAG3 para el cáncer y los trastornos autoinmunes.
«Aunque LAG3 se ha estudiado ampliamente como un posible objetivo inmunomodulador, no se sabía mucho sobre cómo funciona. Realmente era una caja negra», dijo el coautor principal Dario AA Vignali, Ph.D., distinguido profesor y vicepresidente de inmunología de la Facultad de Medicina de la Universidad de Pittsburgh. «Creo que este es un estudio histórico porque finalmente sabemos cómo funciona LAG3. Esto ayudará al desarrollo de nuevas terapias dirigidas a LAG3».
Las células T protegen el cuerpo al eliminar amenazas como el cáncer y las infecciones. Las moléculas llamadas antígenos de las células cancerosas y los patógenos son reconocidas por los receptores de células T, activando estas células inmunitarias para la batalla. Pero las células T agotadas no interactúan normalmente con las células presentadoras de antígenos porque las proteínas del punto de control inmunitario ralentizan las respuestas inmunitarias como los frenos de un automóvil.
Hace más de una década, la investigación sobre dos puntos de control inmunitarios llamados PD-1 y CTLA-4 condujo al desarrollo de medicamentos revolucionarios llamados inhibidores de puntos de control inmunitarios. Estas terapias funcionan liberando los frenos del sistema inmunitario y acelerando la función de las células T.
En marzo de 2022, la Administración de Drogas y Alimentos de EE. UU. aprobó el primer inhibidor de LAG3 para el melanoma avanzado, y otros 18 inhibidores de LAG3 se encuentran en ensayos clínicos, a pesar de la confusión sobre cómo este punto de control inhibe la función de las células T.
Para «mirar debajo del capó» de LAG3, Vignali comenzó esta investigación en su puesto anterior en St. Jude Children’s Research Hospital junto con el primer autor Clifford Guy, Ph.D., quien era un postdoctorado en su laboratorio en ese momento, y co -autor principal Creg Workman, Ph.D., quien ahora es profesor asistente de investigación de inmunología en el laboratorio de Vignali en Pitt.
Cuando las células T interactúan con una célula presentadora de antígeno, forman un punto de contacto llamado sinapsis inmunológica que se inunda con receptores de células T.
«Descubrimos que LAG3 se une a los receptores de células T, pero no los inhibe directamente», explicó Workman. «En cambio, LAG3 usa receptores de células T para llegar a la sinapsis inmunológica».
Usando un tinte especial que mide la acidez, el equipo descubrió que la acumulación de LAG3 en la sinapsis crea condiciones ácidas que interrumpen la asociación entre los correceptores (CD4 en las células T auxiliares o CD8 en las células T asesinas) y una enzima de señalización llamada Lck, lo que frustra un requisito clave para Activación y señalización de células T.
Los fármacos bloqueadores de LAG3 actuales tienen como objetivo una interacción entre LAG3 y las denominadas moléculas MHC Clase II, que se pensaba que eran esenciales para la función de LAG3. Pero el nuevo estudio encontró que la supresión de LAG3 de la actividad de las células T ocurrió con o sin estas moléculas.
«Esta investigación cuestiona el diseño de terapias de bloqueo de LAG en desarrollo», dijo Vignali, quien también es director asociado de estrategia científica y codirector del Programa de Inmunología e Inmunoterapia del Cáncer en el Centro de Cáncer UPMC Hillman. «Obviamente funcionan, pero ¿funcionan de manera óptima? Han sido diseñados para bloquear las interacciones de Clase II, pero este estudio muestra que LAG3 puede funcionar en ausencia de Clase II».
«Ahora que sabemos que LAG3 se une al receptor de células T, podríamos generar bloqueadores óptimos que se dirijan a esta interacción», agregó.
Más allá del cáncer, Vignali dijo que la investigación podría informar nuevos enfoques de tratamiento para trastornos autoinmunes e inflamatorios. Debido a que estas enfermedades son causadas por una respuesta inmune hiperactiva, los medicamentos potenciales podrían mejorar, en lugar de bloquear, la actividad de LAG3.
«Para ayudar al cuerpo a combatir el cáncer, debes liberar los frenos del sistema inmunitario», explicó Vignali. «Pero para la autoinmunidad, debes pisar los frenos con más fuerza».
Otros autores que contribuyeron a esta investigación fueron Diana M. Mitrea, Po-Chien Chou, Jamshid Temirov, Xueyan Liu, Hui Zhang, todos del St. Jude Children’s Research Hospital; Kate M. Vignali, del St. Jude’s Research Hospital, Pitt y UPMC; Richard Kriwacki, del Hospital de Investigación Infantil St. Jude y del Centro de Ciencias de la Salud de la Universidad de Tennessee; Marcel P. Bruchez de la Universidad Carnegie Mellon; y Simon C. Watkins de Pitt.
La investigación revela cómo las células inmunitarias ayudan a los tumores a escapar de las defensas del cuerpo
Clifford Guy et al, LAG3 se asocia con complejos TCR-CD3 y suprime la señalización al impulsar la disociación del co-receptor-Lck, Inmunología de la naturaleza (2022). DOI: 10.1038/s41590-022-01176-4
Citación: La iluminación de la ‘caja negra’ del punto de control inmunológico LAG3 podría producir nuevas terapias contra el cáncer y autoinmunes (18 de abril de 2022) consultado el 18 de abril de 2022 de https://medicalxpress.com/news/2022-04-illumination-immune-checkpoint-lag3- negro.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.