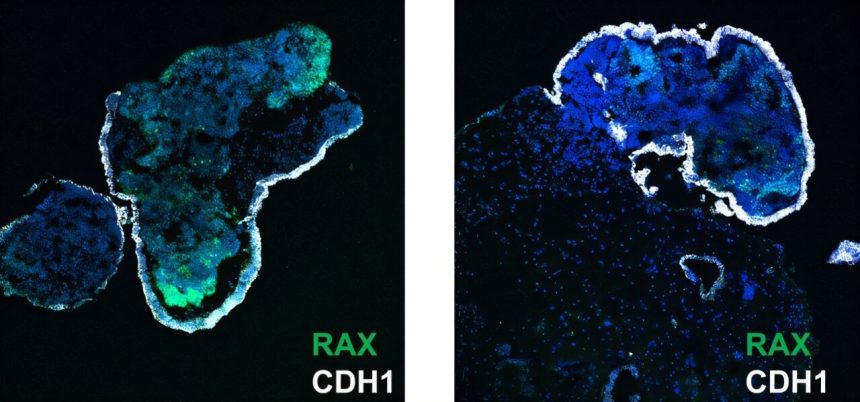
Los organoides que el modelo predijo que serían de alta calidad (izquierda) expresaron RAX (tinción verde) más ampliamente que los organoides que se predijo que serían de baja calidad (derecha). Crédito: Asano et al. (2024) Biología de las Comunicaciones
Los organoides (tejidos en miniatura cultivados en laboratorio que imitan la función y estructura de los órganos) están transformando la investigación biomédica. Prometen avances en trasplantes personalizados, mejores modelos de enfermedades como el Alzheimer y el cáncer, y conocimientos más precisos sobre los efectos de los medicamentos.
Ahora, investigadores de la Universidad de Kyushu y la Universidad de Nagoya en Japón han desarrollado un modelo que utiliza inteligencia artificial (IA) para predecir el desarrollo de organoides en una etapa temprana. El modelo, que es más rápido y preciso que el de los investigadores expertos, podría mejorar la eficiencia y reducir el coste del cultivo de organoides.
En este estudio, publicado en Biología de las Comunicaciones El 6 de diciembre de 2024, los investigadores se centraron en predecir el desarrollo de los organoides hipotalámico-pituitarios.
Estos organoides imitan las funciones de la glándula pituitaria, incluida la producción de hormona adrenocorticotrópica (ACTH): una hormona crucial para regular el estrés, el metabolismo, la presión arterial y la inflamación. La deficiencia de ACTH puede provocar fatiga, anorexia y otros problemas que pueden poner en peligro la vida.
«En nuestro laboratorio, nuestros estudios en ratones muestran que el trasplante de organoides hipotalámico-pituitarios tiene el potencial de tratar la deficiencia de ACTH en humanos», dice el autor correspondiente Hidetaka Suga, profesor asociado de la Facultad de Medicina de la Universidad de Nagoya.
Sin embargo, un desafío clave para los investigadores es determinar si los organoides se están desarrollando correctamente. Derivados de células madre suspendidas en líquido, los organoides son sensibles a pequeños cambios ambientales, lo que resulta en variabilidad en su desarrollo y calidad final.
Los investigadores descubrieron que un signo de buena progresión es la amplia expresión de una proteína llamada RAX en una etapa temprana del desarrollo, que a menudo da como resultado organoides con una fuerte secreción de ACTH más adelante.

Los investigadores utilizaron imágenes fluorescentes para clasificar las imágenes de campo brillante correspondientes, según su expresión RAX, en tres categorías: A (expresión RAX amplia, alta calidad); B (expresión RAX media, calidad media) y C (expresión RAX estrecha, calidad baja). Crédito: Asano et al. (2024) Biología de las Comunicaciones
«Podemos seguir el desarrollo modificando genéticamente los organoides para hacer que la proteína RAX sea fluorescente», dice Suga. «Sin embargo, los organoides destinados a uso clínico, como los trasplantes, no pueden modificarse genéticamente para que sean fluorescentes. Por lo tanto, nuestros investigadores deben juzgar basándose en lo que ven con sus ojos: un proceso inexacto y que requiere mucho tiempo».
Por lo tanto, Suga y sus colegas de Nagoya colaboraron con Hirohiko Niioka, profesor de la Iniciativa de Innovación basada en Datos de la Universidad de Kyushu, para entrenar modelos de aprendizaje profundo para el trabajo.
«Los modelos de aprendizaje profundo son un tipo de IA que imita la forma en que el cerebro humano procesa la información, permitiéndoles analizar y categorizar grandes cantidades de datos mediante el reconocimiento de patrones», explica Niioka.
Los investigadores de Nagoya capturaron imágenes fluorescentes e imágenes de campo brillante (que muestran cómo se ven los organoides bajo luz blanca normal sin ninguna fluorescencia) de organoides con proteínas RAX fluorescentes a los 30 días de desarrollo.
Utilizando las imágenes fluorescentes como guía, clasificaron 1500 imágenes de campo brillante en tres categorías de calidad: A (expresión RAX amplia, alta calidad); B (expresión RAX media, calidad media) y C (expresión RAX estrecha, calidad baja).
Luego, Niioka entrenó dos modelos avanzados de aprendizaje profundo, EfficientNetV2-S y Vision Transformer, desarrollados por Google para el reconocimiento de imágenes, para predecir la categoría de calidad de los organoides. Usó 1200 de las imágenes de campo brillante (400 en cada categoría) como conjunto de entrenamiento.
Después del entrenamiento, Niioka combinó los dos modelos de aprendizaje profundo en un modelo conjunto para mejorar aún más el rendimiento. El equipo de investigación utilizó las 300 imágenes restantes (100 de cada categoría) para probar el modelo de conjunto ahora optimizado, que clasificó las imágenes de campo brillante de organoides con un 70% de precisión.

Se entrenaron dos modelos diferentes de reconocimiento de imágenes, EfficientNetV2-S y Vision Transformer, y luego se combinaron en un modelo conjunto para predecir la calidad de los organoides hipotalámico-pituitarios a partir de imágenes de campo brillante. Crédito: Hirohiko Niioka, Universidad de Kyushu
Por el contrario, cuando investigadores con años de experiencia en cultivo de organoides predijeron la categoría de las mismas imágenes de campo brillante, su precisión fue inferior al 60%.
«Los modelos de aprendizaje profundo superaron a los expertos en todos los aspectos: en precisión, sensibilidad y velocidad», afirma Niioka.
El siguiente paso fue comprobar si el modelo de conjunto también era capaz de clasificar correctamente imágenes de organoides de campo brillante sin modificación genética para hacer que RAX tuviera fluorescencia.
Los investigadores probaron el modelo de conjunto entrenado en imágenes de campo brillante de organoides hipotalámico-pituitarios sin proteínas RAX fluorescentes a los 30 días de desarrollo.
Utilizando técnicas de tinción, descubrieron que los organoides que el modelo clasificó como A (alta calidad) efectivamente mostraban una alta expresión de RAX a los 30 días. Cuando continuaron cultivando, estos organoides luego mostraron una alta secreción de ACTH. Mientras tanto, se observaron niveles bajos de RAX, y más tarde de ACTH, en los organoides que el modelo clasificó como C (baja calidad).
«Por lo tanto, nuestro modelo puede predecir en una etapa temprana de desarrollo cuál será la calidad final del organoide, basándose únicamente en la apariencia visual», dice Niioka. «Hasta donde sabemos, esta es la primera vez en el mundo que se utiliza el aprendizaje profundo para predecir el futuro del desarrollo de organoides».
En el futuro, los investigadores planean mejorar la precisión del modelo de aprendizaje profundo entrenándolo en un conjunto de datos más grande. Pero incluso con el nivel actual de precisión, el modelo tiene profundas implicaciones para la investigación actual de organoides.
«Podemos seleccionar rápida y fácilmente organoides de alta calidad para trasplantes y modelos de enfermedades, y reducir el tiempo y los costos identificando y eliminando organoides que se están desarrollando peor», concluye Suga. «Es un punto de inflexión».
Más información:
Un enfoque de aprendizaje profundo para predecir resultados de diferenciación en organoides hipotalámico-hipofisarios, Biología de las Comunicaciones (2024). DOI: 10.1038/s42003-024-07109-1
Citación: La IA supera a los expertos en la predicción de la calidad futura de los ‘miniórganos’ (2024, 6 de diciembre) recuperado el 6 de diciembre de 2024 de https://medicalxpress.com/news/2024-12-ai-experts-future-quality-mini.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.