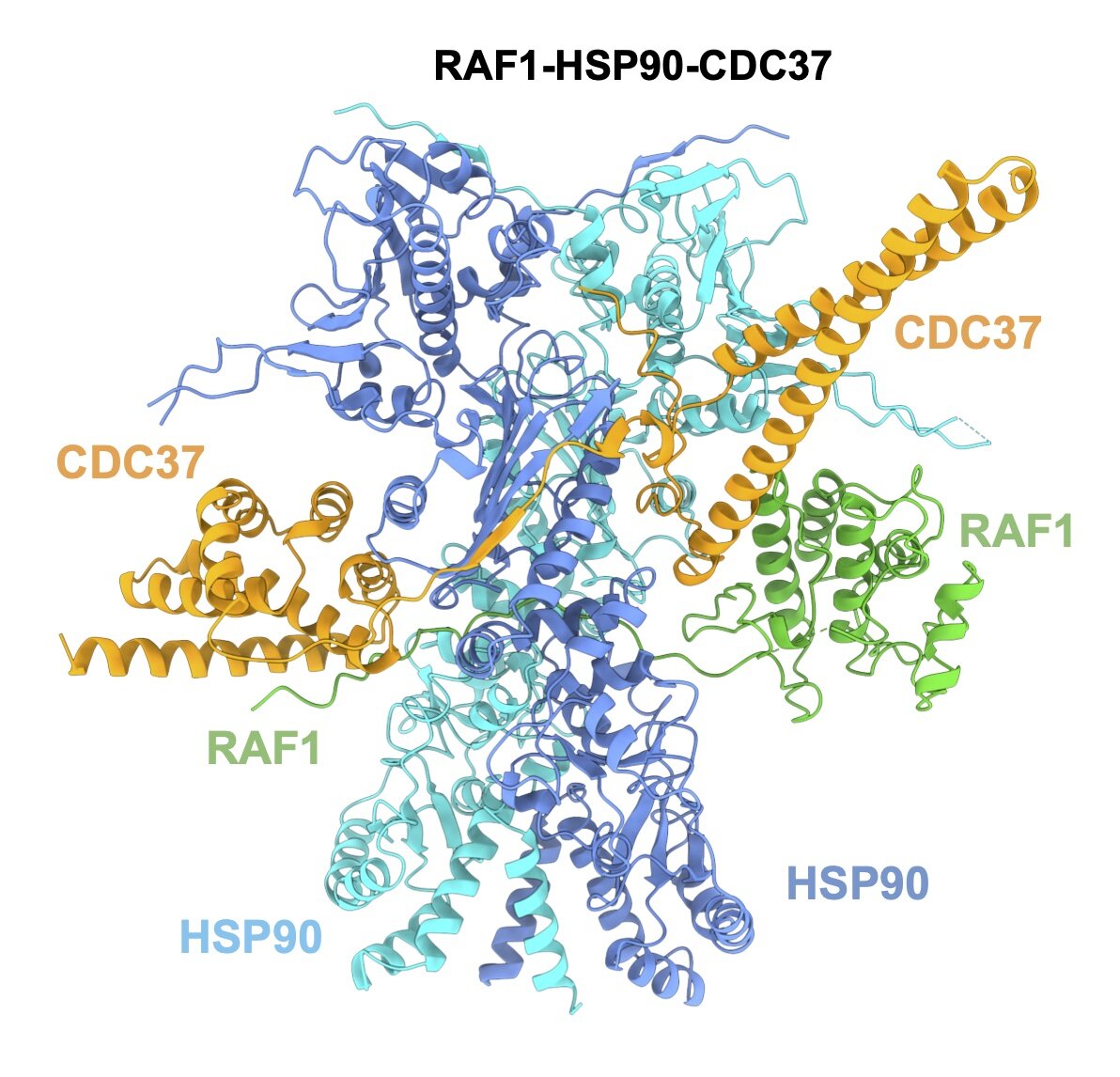
RAF1. Crédito: CNIO
Uno de los principales retos en oncología es el desarrollo de fármacos contra los oncogenes KRAS. Estos oncogenes, genes que causan cáncer cuando mutan, son responsables de una cuarta parte de todos los cánceres humanos, incluidos los tres tipos de tumores con las tasas de mortalidad más altas: adenocarcinoma de pulmón, carcinoma colorrectal y adenocarcinoma ductal pancreático.
Aunque los oncogenes KRAS ya fueron descubiertos por el grupo de Mariano Barbacid hace cuatro décadas, el primer fármaco contra ellos, Sotorasib, Amgen, ha sido aprobado por la FDA hace apenas un año. A pesar de la importancia de este hito, Sotorasib actúa solo contra los tumores que portan una de las múltiples mutaciones presentes en los oncogenes KRAS y, por lo tanto, su impacto clínico es limitado. Además, los pacientes tratados con este fármaco desarrollan resistencia a los pocos meses de tratamiento.
RAF1 y adenocarcinoma de pulmón
Más allá del desarrollo de fármacos contra KRAS, una de las áreas de investigación más activas en este momento busca identificar inhibidores de proteínas, como RAF1, responsables de transmitir las señales oncogénicas de KRAS.
En este sentido, el laboratorio de Mariano Barbacid, utilizando modelos de ratón genéticamente modificados que recapitulan fielmente los adenocarcinomas de pulmón humanos, demostró hace cuatro años que la eliminación de la proteína RAF1 inducía la regresión de la mayoría de los tumores sin efectos tóxicos significativos.
Objetivo: degradar RAF1
Estas observaciones han generado un enorme interés por encontrar fármacos capaces de degradar RAF1. Los resultados de un nuevo estudio, publicado hoy en Célula Molecularabren una ventana de oportunidad para diseñar degradadores de RAF1 que, solos o en combinación con inhibidores de KRAS, podrían generar un importante efecto terapéutico en pacientes con adenocarcinoma de pulmón inducido por oncogenes KRAS.
La determinación de la estructura tridimensional de RAF1 es un paso clave para lograr este objetivo, ya que revela las partes de la proteína a las que podría anclarse químicamente un fármaco y promover su destrucción por la maquinaria celular (las células tienen mecanismos de limpieza que degradan proteínas defectuosas o inútiles).
Los principales investigadores responsables de este trabajo son Sara García-Alonso, del CNIO, y Pablo Mesa, del grupo de Biología Molecular y Estructural de la Universidad de Copenhague.
“La información que aporta este estudio abre un abanico de opciones para desarrollar fármacos que puedan degradar RAF1”, afirma García-Alonso. «Ahora se abre una ventana de oportunidad para diseñar degradadores RAF1 con un importante efecto terapéutico en pacientes con adenocarcinoma de pulmón inducido por oncogenes KRAS».
Investigadores desarrollan una estrategia eficaz contra tumores de pulmón mutantes KRAS en ratones
Sara García-Alonso et al, Estructura del complejo RAF1-HSP90-CDC37 revela la base de la regulación RAF1, Célula Molecular (2022). DOI: 10.1016/j.molcel.2022.08.012
Citación: La estructura de la proteína RAF1 revelada: Un paso clave en el desarrollo de nuevos fármacos contra el cáncer de pulmón (1 de septiembre de 2022) recuperado el 1 de septiembre de 2022 de https://medicalxpress.com/news/2022-09-protein-raf1-revealed -drogas-clave.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.