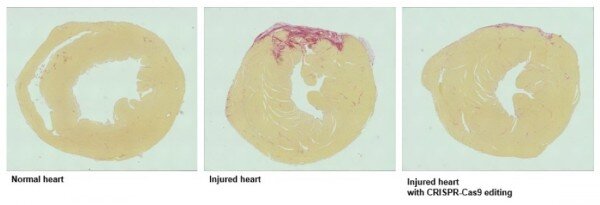
La figura muestra secciones transversales de corazones de ratón con áreas dañadas en rojo. El tratamiento con componentes CRISPR que expresan virus reduce el daño cardíaco después de una lesión isquémica. Crédito: UT suroeste
La edición de un gen que provoca una cascada de daños después de un ataque cardíaco pareció revertir este curso inevitable en ratones, dejando sus corazones notablemente ilesos, según mostró un nuevo estudio realizado por científicos de UT Southwestern. Los hallazgos, publicados en Cienciapodría conducir a una nueva estrategia para proteger a los pacientes de las consecuencias de las enfermedades del corazón.
«Por lo general, privar al corazón de oxígeno durante un período prolongado, como sucede a menudo en un ataque al corazón, lo dañará sustancialmente. Pero aquellos animales cuyos músculos del corazón fueron sometidos a la edición de genes después de los ataques cardíacos inducidos parecen ser esencialmente normales en las semanas y meses después», dijo Eric Olson, Ph.D., Director del Centro Hamon para la Medicina y la Ciencia Regenerativa y Presidente de Biología Molecular en la UTSW, quien codirigió el estudio con Rhonda Bassel-Duby, Ph.D., Profesora de Biología Molecular.
Desde su descubrimiento hace una década, los científicos han utilizado el sistema de edición de genes CRISPR-Cas9 para corregir las mutaciones genéticas responsables de la enfermedad, incluido el trabajo del laboratorio Olson sobre la distrofia muscular de Duchenne. Sin embargo, explicó el Dr. Bassel-Duby, estas enfermedades causadas por mutaciones afectan a grupos relativamente pequeños de personas, mientras que las enfermedades no genéticas afectan a un número mucho mayor. Por ejemplo, las enfermedades cardiovasculares son la principal causa de muerte en todo el mundo y matan a unos 19 millones de personas cada año.
Los investigadores descubrieron recientemente que gran parte del daño de un ataque cardíaco, un evento caracterizado por el bloqueo de los vasos sanguíneos que alimentan el corazón, privándolo de oxígeno, es causado por la sobreactivación de un gen llamado CaMKIIδ. Este gen desempeña una variedad de funciones en la señalización y función de las células cardíacas. La sobreactivación ocurre cuando el corazón está estresado, provocado por la oxidación de dos aminoácidos de metionina que forman parte del CaMKIIδ proteína.
Dres. Olson y Bassel-Duby y sus colegas razonaron que si estas metioninas pudieran convertirse en un aminoácido diferente, no se produciría la oxidación, lo que evitaría que el corazón CaMKIIδ sobreactivación y daño posterior después de un ataque al corazón.
Para probar esta idea, Simon Lebek, MD, becario postdoctoral y otros miembros del equipo utilizaron CRISPR-Cas9 para editar CaMKIIδ en células cardíacas humanas que crecen en una placa de Petri. Las pruebas mostraron que cuando las células del corazón sin editar se colocaron en una cámara con poco oxígeno, desarrollaron numerosos marcadores de daño y posteriormente murieron. Sin embargo, las células editadas se protegieron del daño y sobrevivieron.
Luego, los investigadores probaron un experimento similar en ratones vivos, induciendo un ataque cardíaco en estos animales al restringir el flujo sanguíneo a la cámara de bombeo principal de su corazón durante 45 minutos y luego administrar CaMKIIδ componentes de edición de genes directamente a los corazones de algunos animales. Tanto los ratones que recibieron edición de genes como los que no tuvieron una función cardíaca gravemente comprometida en las primeras 24 horas después de sus ataques cardíacos. Pero mientras que los ratones sin la edición de genes continuaron empeorando con el tiempo, los que recibieron la edición de genes mejoraron constantemente durante las próximas semanas, logrando finalmente una función cardíaca que era casi indistinguible de antes de sus ataques cardíacos.
Investigaciones posteriores mostraron que la edición de genes parecía estar aislada del corazón; no había evidencia de edición CaMKIIδ en otros órganos, incluidos el hígado, el cerebro o los músculos. No se observaron efectos secundarios negativos casi un año después del tratamiento, los Dres. dijeron Olson y Bassel-Duby. El tratamiento también pareció ser duradero, agregaron, y señalaron que los ratones modificados genéticamente podían hacer ejercicio intenso de manera similar a los ratones que nunca habían tenido ataques cardíacos.
Aunque este tratamiento necesitará estudios sustanciales de seguridad y eficacia antes de que pueda usarse en humanos, los investigadores sugieren que la edición de genes podría ofrecer una solución prometedora para el tratamiento de pacientes después de un ataque cardíaco y podría tener potencial para una variedad de otras enfermedades no genéticas. .
«En lugar de apuntar a una mutación genética, esencialmente modificamos un gen normal para asegurarnos de que no se vuelva hiperactivo de manera dañina. Es una nueva forma de usar la edición de genes CRISPR-Cas9», dijo el Dr. Bassel-Duby.
El Dr. Olson ocupa la Cátedra Distinguida Pogue en Investigación de Defectos Congénitos Cardíacos, la Cátedra Distinguida Robert A. Welch en Ciencias y la Cátedra Annie y Willie Nelson en Investigación de Células Madre.
Otros investigadores de UTSW que contribuyeron a este estudio incluyen a Francesco Chemello, Xurde M. Caravia, Wei Tan, Hui Li, Kenian Chen, Lin Xu y Ning Liu.
Más información:
Simon Lebek et al, Ablación de la oxidación de CaMKIIδ mediante la edición de base CRISPR-Cas9 como terapia para la enfermedad cardíaca, Ciencia (2023). DOI: 10.1126/ciencia.ade1105
Citación: La edición de genes detiene el daño en ratones después de ataques cardíacos en un nuevo estudio (23 de enero de 2023) recuperado el 23 de enero de 2023 de https://phys.org/news/2023-01-gene-halts-mice-heart.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.