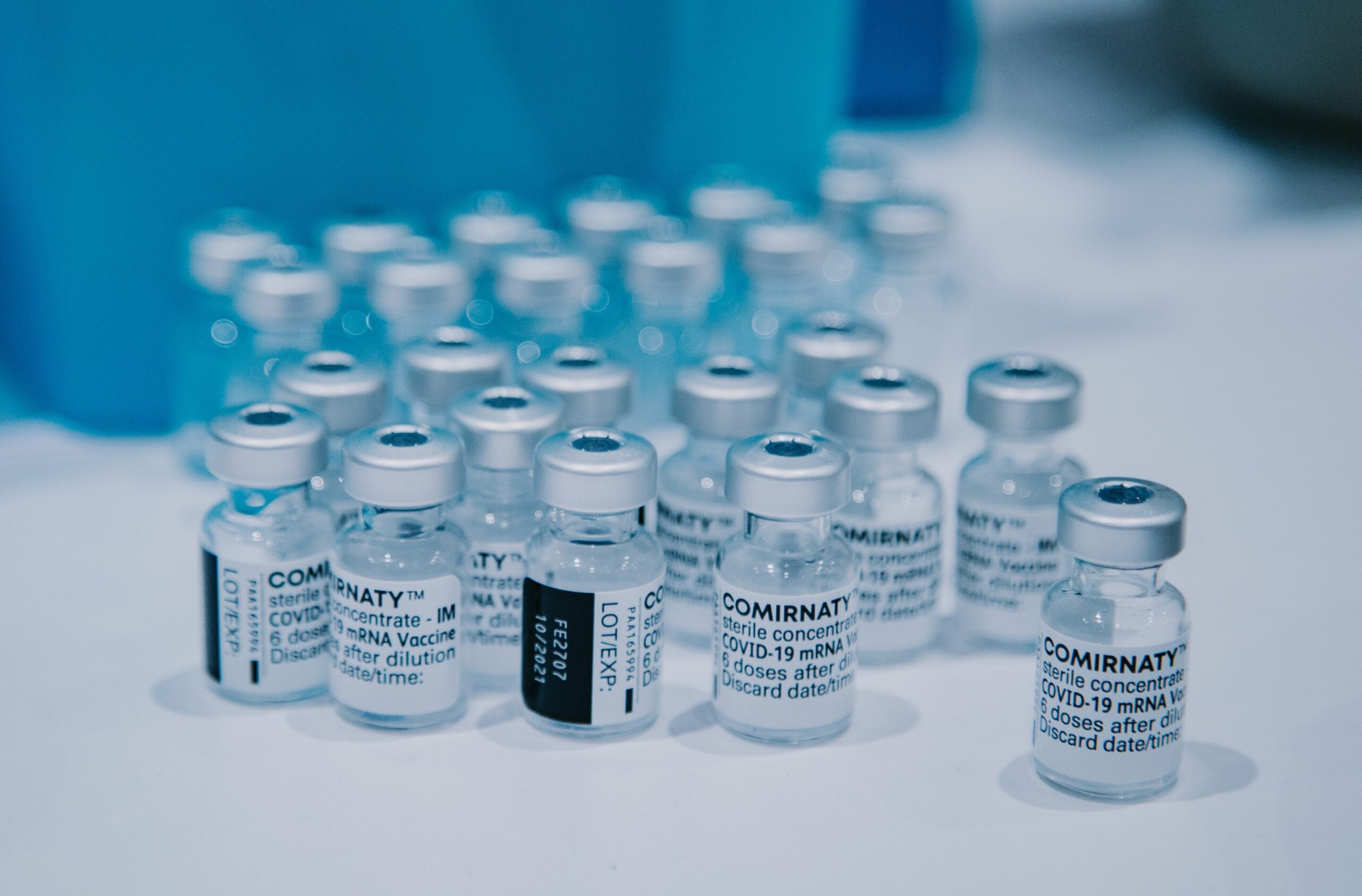
Crédito: Unsplash/CC0 Dominio público
El gran potencial de los sistemas de administración no virales de mRNA y pDNA se ha demostrado en las vacunas contra la enfermedad por coronavirus 2019 (COVID-19). De hecho, dos formulaciones de vacunas de ARNm de Pfizer-BioNTech y Moderna fueron aprobadas para uso de emergencia dentro de un año después del brote pandémico y se han administrado a miles de millones de personas en todo el mundo. Además, una vacuna pDNA desarrollada por Zydus Cadila también obtuvo la aprobación de emergencia en la India y mostró una alta eficiencia para prevenir infecciones en un ensayo clínico grande. Estos ejemplos exitosos impulsan más investigaciones y el desarrollo de vacunas y terapias basadas en mRNA y pDNA. Las áreas objetivo no se limitan a la vacunación preventiva para enfermedades infecciosas, sino que se amplían a las vacunas terapéuticas contra el cáncer, la edición del genoma y la terapia de reemplazo de proteínas.
Sin embargo, los sistemas no virales actuales necesitan mejoras. Por ejemplo, los efectos adversos relativamente intensos de las vacunas de ARNm, incluida la miocarditis, provocan dudas sobre la vacuna y debates sobre el refuerzo repetido. Por lo tanto, se demandan formulaciones más seguras para que las vacunas de ARNm se conviertan en plataformas para diversas enfermedades infecciosas. Mientras tanto, las vacunas terapéuticas contra el cáncer requieren formulaciones más eficientes para superar la naturaleza inmunosupresora de los cánceres. Para otras aplicaciones, incluida la edición del genoma y la terapia de reemplazo de proteínas, los portadores de entrega deben llegar a tejidos específicos e introducir pDNA y mRNA sin dañar los tejidos.
El desarrollo de sistemas de entrega no virales tiene dos direcciones. Uno se centra en la mejora general de los procesos de administración, que incluye la prevención de la degradación extracelular del mRNA y el pDNA por parte de las nucleasas, el direccionamiento intracelular del mRNA y el pDNA a los sitios deseados y la prolongación de la expresión de la proteína del mRNA y el pDNA. En la otra dirección, los sistemas de administración se ajustan para fines específicos, como llegar a tejidos y células particulares para lograr objetivos terapéuticos y estimular los sistemas inmunitarios innatos cuando se usan en vacunas.
El Prof. Satoshi Uchida (Científico de Investigación Principal, Centro de Innovación de NanoMedicina), quien también es Profesor Asociado de la Universidad de Medicina de la Prefectura de Kioto, publicó una revisión de un artículo sobre la entrega de ARN mensajero no viral (ARNm) y ADN plasmídico (pADN) abordando las diversas tecnologías de entrega de mRNA y pDNA, desde la investigación básica hasta la aplicación terapéutica y clínica en Farmacia.
Este documento proporciona revisiones exhaustivas de la entrega de mRNA y pDNA no viral al abordar las diversas tecnologías de entrega de mRNA y pDNA, desde la investigación básica hasta la aplicación terapéutica y clínica.
El nuevo estudio de la vacuna de ARNm del VIH recibe impulso del desarrollo de la vacuna de ARNm de COVID
Satoshi Uchida, Sistemas de suministro de ADN plásmido y ARN mensajero para terapias avanzadas, Farmacia (2022). DOI: 10.3390/productos farmacéuticos 14040810
Proporcionado por el Centro de Innovación de NanoMedicine
Citación: Explorando los sistemas de entrega de ADN plasmídico y ARN mensajero para terapias avanzadas (15 de abril de 2022) recuperado el 16 de abril de 2022 de https://medicalxpress.com/news/2022-04-exploring-delivery-plasmid-dna-messenger.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.