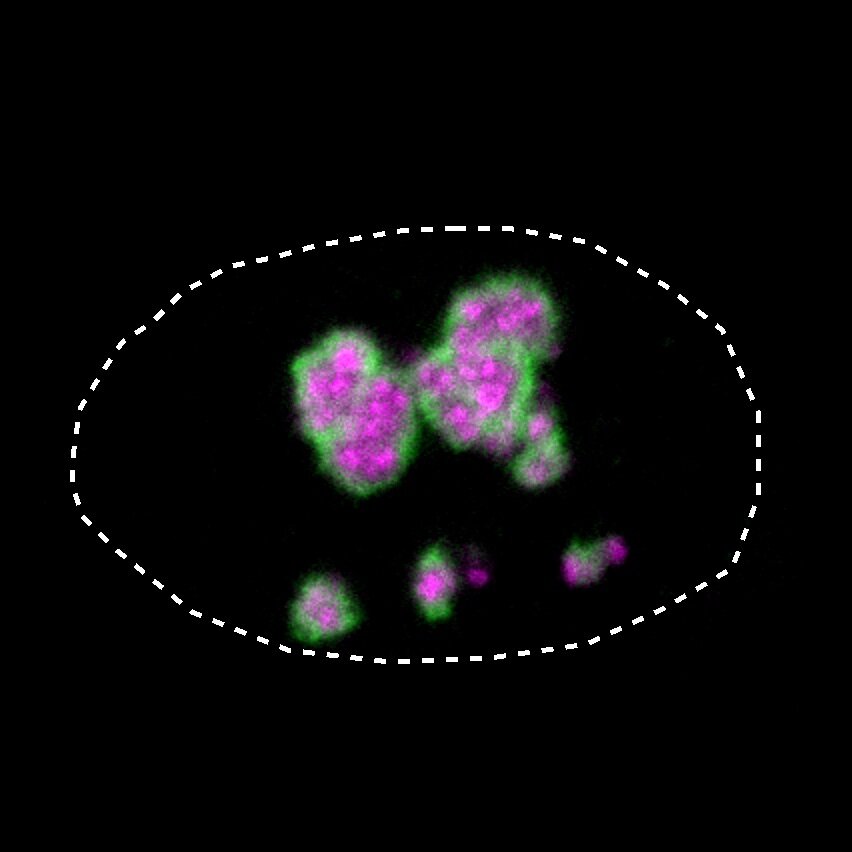
Núcleo (línea de puntos) de una célula humana. La proteína HMGB1 (verde) que está mutada en el síndrome BPTA forma una capa dura en el nucléolo (rosa), lo que provoca el trastorno del desarrollo. Crédito: MPIMG | henri niskanen
Universitätsmedizin Berlin, el Instituto Max Planck de Genética Molecular (MPIMG) y el Hospital Universitario Schleswig-Holstein (UKSH) han investigado en detalle cómo surge el síndrome BPTA, una condición hereditaria extremadamente rara. Un cambio en la carga de una proteína interrumpe la autoorganización celular, lo que resulta en un trastorno del desarrollo.
El equipo también identificó cientos de cambios genéticos comparables asociados con diversas afecciones, como trastornos del desarrollo cerebral y predisposición al cáncer. Este mecanismo, que ahora ha sido descrito en la revista Naturalezapodría ser la causa de numerosas enfermedades y condiciones de salud inexplicables.
Miles de cambios genéticos están asociados con diversas enfermedades, trastornos y condiciones. Pero rara vez está claro cómo, exactamente, estas mutaciones producen enfermedades. Esto se debe a que los cambios se relacionan con secciones de proteínas con una estructura tridimensional desordenada y una función dentro de la célula de la que hasta ahora se sabe poco.
«Es difícil estudiar de qué se encargan estos tipos de segmentos de proteínas porque, en muchos casos, tienen que interactuar con otras moléculas antes de producir sus efectos», dice el Dr. Martin Mensah, del Instituto de Genética Médica y Humana de Charité. Es uno de los dos primeros autores del estudio y miembro del Programa Científico Clínico Digital, que Charité opera con el Instituto de Salud de Berlín (BIH) en Charité.
«Tomando el síndrome BPTA como ejemplo, ahora hemos descrito en detalle cómo los cambios en las áreas desordenadas de las proteínas pueden causar una enfermedad genética». Esto significa que el equipo de investigación ha descubierto un nuevo mecanismo que causa enfermedades hereditarias y, según el estudio, uno que sorprendentemente no es tan raro después de todo.
BPTA significa «braquifalangia, polidactilia y aplasia/hipoplasia tibial». Los pacientes tienen malformaciones graves que afectan las extremidades, la cara, el sistema nervioso y los huesos, y otros órganos. Hay menos de diez casos documentados en todo el mundo, lo que hace que esta enfermedad sea extremadamente rara.
Para identificar la causa de este síndrome, los investigadores descodificaron la información genética de cinco de los pacientes afectados y descubrieron un cambio en la proteína HMGB1 en todos ellos. Debido a lo que se conoce como mutación de cambio de marco, el tercio final de la estructura de la proteína tiene una carga positiva en lugar de la negativa habitual.
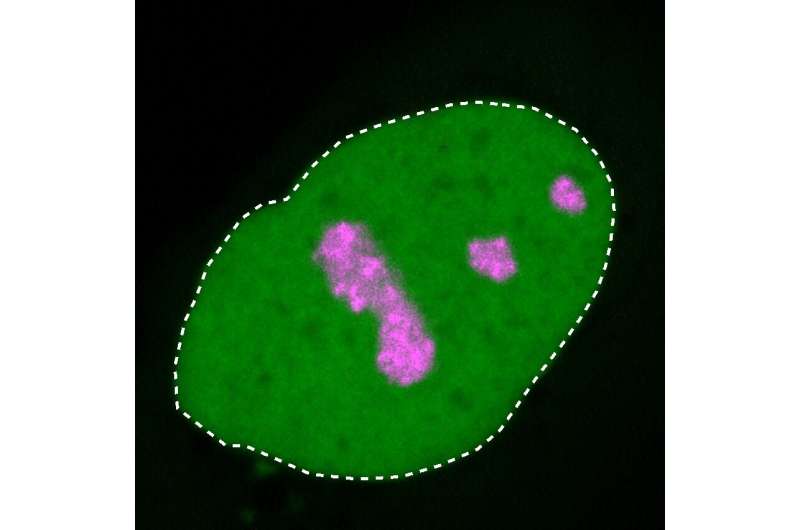
Núcleo de una célula humana. La proteína HMGB1 (verde) normalmente se distribuye por todo el núcleo de la célula (línea de puntos). Rosa: Nucléolo. Crédito: MPIMG | henri niskanen
El nucléolo se solidifica
El cambio en la carga significa que HMGB1 se parece a las proteínas que tienden a agruparse en el nucléolo, una pequeña área en el núcleo de la célula donde se ensamblan partes de las fábricas de proteínas de la célula.
Este papel hace que el nucléolo sea crucial para la viabilidad de una célula. Como demostró el equipo de investigación en base a experimentos con proteínas aisladas y cultivos celulares, la proteína HMGB1 mutada, que ahora tiene una sección final cargada positivamente, se atrae incorrectamente hacia el nucléolo. Y debido a que la extensión de la proteína también se ha vuelto más rígida, la proteína HMGB1 también se agrupa.
«Bajo un microscopio, pudimos ver que esto hace que el nucléolo pierda sus propias propiedades líquidas y se vuelva cada vez más rígido», explica el Dr. Henri Niskanen, investigador de MPIMG y otro primer autor del estudio.
Esta solidificación del nucléolo afecta negativamente al funcionamiento vital de las células. Murieron más células con la proteína mutada que sin la mutación en el cultivo. El Prof. Dr. Malte Spielmann, Director del Instituto de Genética Humana de UKSH y uno de los tres autores principales del estudio, ofrece su conclusión: «Mostramos cómo las mutaciones en secciones desordenadas de proteínas pueden causar una enfermedad. Cuando hay un cambio en la carga, la proteína se acumula erróneamente en el nucléolo, afectando negativamente su funcionamiento vital, lo que conduce a un trastorno en el desarrollo del organismo”.
Nuevas explicaciones para enfermedades existentes
Tras sus hallazgos iniciales, los investigadores buscaron en bases de datos que contenían las secuencias de ADN de miles de personas, en busca de casos similares. Pudieron identificar más de 600 mutaciones en 66 proteínas que dieron a la parte final de la proteína una carga positiva y propiedades más rígidas. De esas mutaciones, 101 se habían asociado previamente con varias enfermedades, incluidos trastornos del neurodesarrollo y una mayor susceptibilidad al cáncer.
Para 13 proteínas seleccionadas, el equipo estudió el cultivo celular para ver si las mutaciones les daban una afinidad particular por el nucléolo. Ese fue el caso de 12 de ellos. Aproximadamente la mitad de las proteínas analizadas afectaron el funcionamiento del nucléolo, por lo que eran similares al mecanismo de enfermedad encontrado para el síndrome BPTA.
«El mecanismo que causa esta enfermedad, que descubrimos en el síndrome de BPTA, también podría estar implicado en muchas otras enfermedades y afecciones», dice la Prof. Dra. Denise Horn, autora principal del estudio que trabaja en el Instituto de Medicina y Salud Humana. Genética en Charité. «Así que hemos abierto una puerta que podría ayudar a explicar muchas otras enfermedades. El verdadero trabajo comienza ahora».
El mecanismo recientemente identificado también podría conducir a nuevos enfoques terapéuticos, al menos para algunas enfermedades. «Los tumores son atribuibles a cambios genéticos en las células afectadas», explica el Dr. Denes Hnisz, jefe de un grupo de investigación de MPIMG y tercer autor principal del estudio. «Esto significa que podemos prevenir el desarrollo del cáncer en el futuro al intervenir en la autoorganización de la célula, que está mediada por secciones desordenadas de proteínas».
Más información:
Denes Hnisz, Separación de fases aberrante y disfunción nucleolar en enfermedades genéticas raras, Naturaleza (2023). DOI: 10.1038/s41586-022-05682-1. www.nature.com/articles/s41586-022-05682-1
Citación: Examen del mecanismo causal detrás de enfermedades hereditarias raras (8 de febrero de 2023) consultado el 8 de febrero de 2023 de https://medicalxpress.com/news/2023-02-causal-mechanism-rare-hereditary-diseases.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.