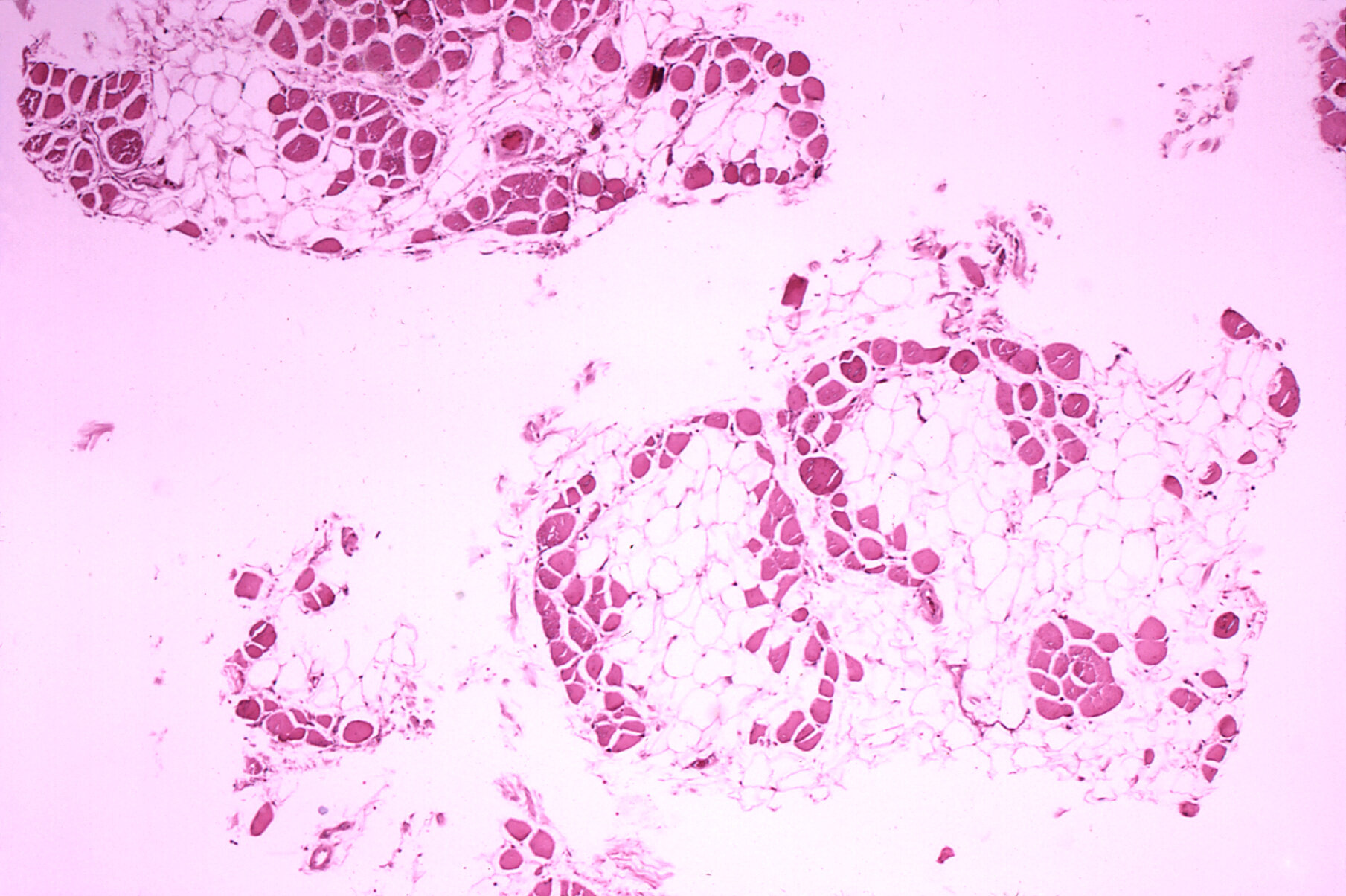
Histopatología del músculo gastrocnemio de un paciente que falleció por distrofia muscular pseudohipertrófica, tipo Duchenne. La sección transversal del músculo muestra un extenso reemplazo de fibras musculares por células adiposas. Crédito: Wikimedia Commons/dominio público
Una terapia celular desarrollada por el director ejecutivo del Smidt Heart Institute estabiliza los músculos debilitados, incluido el músculo cardíaco, en pacientes con distrofia muscular de Duchenne, según un nuevo estudio publicado en la revista internacional revisada por pares. La lanceta espectáculos
Si el éxito del estudio HOPE-2 se duplica en el próximo ensayo clínico multicéntrico, aleatorizado y controlado con placebo HOPE-3, la terapia celular intravenosa podría convertirse en el primer tratamiento aprobado por la Administración de Alimentos y Medicamentos para pacientes con Duchenne con enfermedad avanzada.
«Esta terapia es única porque aborda dos necesidades vitales de los pacientes con Duchenne: movimiento físico y un corazón sano», dijo Eduardo Marbán, MD, Ph.D., director ejecutivo del Smidt Heart Institute en Cedars-Sinai, el Mark S. Siegel Family Foundation Profesor distinguido, autor del estudio e inventor de las células derivadas de la cardiosfera (CDC), células progenitoras derivadas del tejido cardíaco humano, que se han utilizado en múltiples ensayos clínicos.
La distrofia muscular de Duchenne es un trastorno hereditario raro que afecta principalmente a los hombres. Es causado por mutaciones en un gen en el cromosoma X que interfiere con la producción de una proteína llamada distrofina que los músculos necesitan para funcionar. Los niños que nacen con tales mutaciones tienen debilidad muscular en todo el cuerpo. Esto les dificulta realizar actividades normales como correr, saltar, subir escaleras, levantarse después de estar sentados y pedalear en bicicleta. También pueden enfermarse gravemente cuando se debilitan los músculos del corazón y los órganos respiratorios.
El pronóstico para los pacientes con distrofia muscular de Duchenne es sombrío. La mayoría usa una silla de ruedas cuando son adolescentes y, por lo general, no llegan a los 30 años. No hay cura para la enfermedad. Actualmente, los únicos tratamientos médicos aprobados están dirigidos a retrasar la pérdida de la capacidad para caminar; no hay nada disponible para pacientes con enfermedad más avanzada, que ahora superan en número a aquellos con síntomas más leves.
«El ensayo HOPE-2 cambia las reglas del juego para la distrofia muscular», dijo Craig M. McDonald, MD, investigador principal del ensayo y profesor y presidente de medicina física y rehabilitación y profesor de pediatría de la Universidad de California, Davis Health, uno de varios sitios que participan en el ensayo. «Por primera vez, tenemos un tratamiento que retarda notablemente la pérdida de la función del brazo y preserva la función cardíaca en pacientes con Duchenne. Las células se administran por vía intravenosa y solo cuatro veces al año, por lo que el tratamiento no es una carga para los pacientes y sus familias. «
Otras terapias experimentales tienen como objetivo hacer que el cuerpo produzca distrofina. La terapia estudiada en este ensayo clínico de Fase II tiene un enfoque diferente. Utiliza células cardíacas llamadas cardioesferas, o CDC, que son un tipo de células progenitoras derivadas del tejido cardíaco humano, para mejorar la función del músculo esquelético y el corazón, al menos en parte al mitigar la inflamación. El músculo esquelético media el movimiento voluntario, como el de los brazos, mientras que el corazón bombea sangre por todo el cuerpo para mantener la vida.
«Este enfoque terapéutico hace posible que todas las personas con DMD se beneficien independientemente de su mutación genética exacta, que puede variar de un niño a otro», dijo Marbán. «El hecho de que las células ayuden tanto al corazón como al músculo esquelético es notable, ya que ningún otro tratamiento lo ha hecho».
El ensayo fue patrocinado por Capricor Therapeutics, una empresa de biotecnología con sede en San Diego, que posee una licencia mundial exclusiva para esta tecnología y propiedad intelectual y fabrica el tratamiento celular con el nombre de producto CAP-1002.
«Estamos muy animados por los resultados del estudio HOPE-2», dijo Linda Marbán, Ph.D., directora ejecutiva de Capricor. «Ahora hemos realizado HOPE-Duchenne y HOPE-2, los ensayos clínicos de Fase I y Fase II utilizando CAP-1002 para tratar a pacientes con DMD en etapa tardía. Estos mostraron mejoras estadísticamente significativas en la función cardiaca o de las extremidades superiores en los grupos de tratamiento Estamos en el proceso de iniciar un estudio fundamental de Fase III, llamado HOPE-3, que la FDA ha señalado como el siguiente paso hacia la aprobación del producto para la grave necesidad insatisfecha de la DMD».
El estudio incluyó a 20 niños de varios hospitales de los EE. UU. Todos tenían 10 años o más y todos tenían distrofia muscular de Duchenne.
Cada paciente en el ensayo tenía lo que los investigadores clasificaron como «deterioro moderado de las extremidades superiores», lo que significa que su función variaba desde poder levantar ambos brazos simultáneamente por encima de la cabeza flexionando el codo hasta poder llevar una o dos manos a la boca, pero no le traigas una copa.
«Los niños con DMD eventualmente se vuelven dependientes de sus brazos para la mayoría de sus actividades, como comer y operar su silla de ruedas», dijo McDonald. «Cualquier mejora en la función de las extremidades superiores puede marcar una gran diferencia».
Ocho niños fueron asignados al azar para recibir la terapia celular y 12 fueron asignados al azar para recibir el placebo. Las células y el placebo se administraron por vía intravenosa cada tres meses durante un año. El estudio fue doble ciego, lo que significa que ni los médicos ni los pacientes sabían quién estaba recibiendo el tratamiento o el placebo.
Los resultados mostraron que los pacientes que recibieron CAP-1002 experimentaron menos pérdida de capacidad en las extremidades superiores después de 12 meses que los pacientes que recibieron el placebo. Aunque los niños que recibieron CAP-1002 aún perdieron parte del movimiento de las extremidades superiores durante ese período, lo hicieron a un ritmo un 71 % más lento que los niños que no recibieron la terapia.
La función cardíaca también mejoró en los niños que recibieron la terapia basada en células en comparación con el placebo, un hallazgo importante dado que la insuficiencia cardíaca es la principal causa de muerte en personas con distrofia muscular de Duchenne.
El nuevo Lanceta El estudio es el último en el cuerpo de trabajo de Marbán que aprovecha los CDC para mejorar la función cardíaca. Los resultados del ensayo anterior CADUCEUS, publicado en La lanceta en 2014, mostró que la infusión de CDC en los corazones de los sobrevivientes de un ataque cardíaco redujo significativamente las cicatrices del ataque cardíaco. El presente estudio utiliza la entrega de células por vía intravenosa, que es mucho más fácil que la infusión cardíaca.
El tratamiento parece ser seguro. Un niño experimentó una reacción alérgica grave a CAP-1002 durante una segunda infusión intravenosa y requirió una inyección de epinefrina y hospitalización. Después de eso, los investigadores pusieron a los niños en un régimen de medicamentos previo al tratamiento para reducir el riesgo de reacciones alérgicas. Solo un niño experimentó una reacción alérgica después de que esto se implementó y no requirió medicación ni hospitalización.
Se necesitan más estudios para saber si los efectos de esta terapia duran más de 12 meses y prolongan la vida de los niños con DMD.
«Aquí mostramos la promesa de la terapia celular en la prevención de la progresión de la enfermedad cardíaca en una enfermedad genética rara, pero hay buenas razones para creer que tal terapia algún día puede usarse para formas más comunes de insuficiencia cardíaca», dijo Marbán.
La terapia celular mejora los signos y síntomas de la distrofia muscular de Duchenne
Craig M McDonald et al, Terapia celular derivada de la cardiosfera intravenosa repetida en la distrofia muscular de Duchenne en etapa tardía (HOPE-2): un ensayo de fase 2 multicéntrico, aleatorizado, doble ciego, controlado con placebo, La lanceta (2022). DOI: 10.1016/S0140-6736(22)00012-5
Citación: El tratamiento celular ralentiza la enfermedad en pacientes con distrofia muscular de Duchenne (13 de abril de 2022) recuperado el 14 de abril de 2022 de https://medicalxpress.com/news/2022-04-cell-treatment-disease-duchenne-muscular.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.