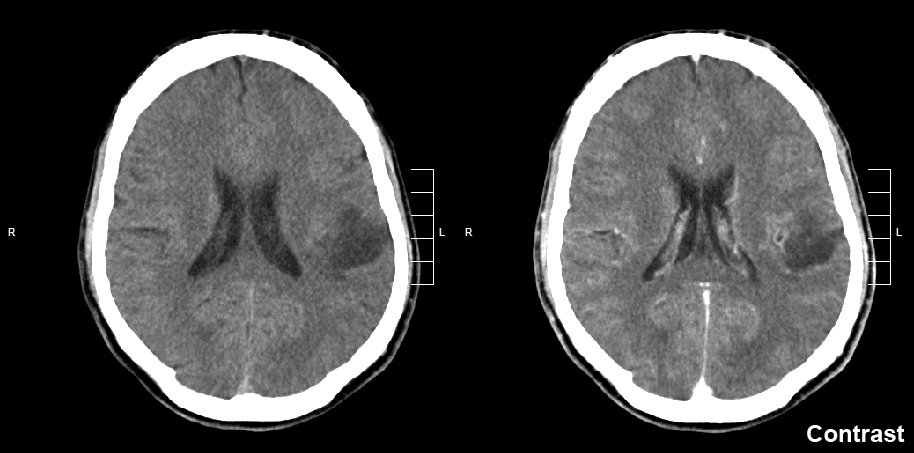
Glioma del lóbulo parietal izquierdo. Tomografía computarizada con realce de contraste. Crédito: Mikhail Kalinin/CC BY-SA 3.0
Los investigadores han identificado una variedad de alteraciones genéticas en los cánceres cerebrales de glioma que les ayudarán a comprender cómo las diferentes mutaciones en un gen en particular interactúan con otras alteraciones genéticas y cuáles son más susceptibles a los tratamientos dirigidos en adultos.
Al presentar los resultados del grupo más grande de pacientes con glioma hasta la fecha, la Dra. Karisa Schreck le dirá al 34º Simposio EORTC-NCI-AACR sobre objetivos moleculares y terapéutica del cáncer en Barcelona, España, que aunque las diferentes alteraciones en el gen BRAF, que pueden conducir el desarrollo del glioma, eran bien entendidos en los gliomas que ocurren en niños, este no era el caso de los adultos.
La Dra. Schreck, profesora asistente de neurología en la Facultad de Medicina de la Universidad Johns Hopkins, Baltimore, EE. UU., dice que su investigación se centra en el desarrollo de una terapia dirigida para el glioma con mutación BRAF. Cuando comenzó a diseñar su primer ensayo clínico, se dio cuenta de la amplitud de las mutaciones BRAF en adultos con cáncer de cerebro y no se entendía bien cómo responden a la quimioterapia tradicional. Su cohorte de pacientes, la más grande que ella sepa, le permite comenzar a responder estas preguntas y le permitirá diseñar ensayos clínicos mejor informados para estos pacientes.
Las alteraciones de BRAF son importantes para identificar en los tumores cerebrales porque pueden determinar el tratamiento. Sin embargo, no está claro qué tipos de alteraciones BRAF ocurren en adultos con glioma y si las alteraciones BRAF específicas están asociadas con otras alteraciones genéticas o con un curso clínico diferente.
El término «glioma» cubre varios tipos de tumores que se originan en las células gliales del cerebro. El glioblastoma es el tipo más común en adultos y niños, ocurre en 3,23 por 100 000 de la población, y solo el 7 % de los pacientes con glioblastoma sobrevive cinco años después del diagnóstico. Se necesitan con urgencia tratamientos nuevos y mejores, y se han desarrollado fármacos que se dirigen a mutaciones BRAF específicas, como dabrafenib y trametinib, que inhiben el BRAF.v600E mutación. Saber qué mutación o combinación de alteraciones genéticas están provocando el cáncer de un paciente es crucial para elegir la mejor terapia que tenga más probabilidades de prolongar la supervivencia.
El Dr. Schreck y sus colegas recolectaron datos de Dana-Farber/Harvard Cancer Center, Johns Hopkins Hospital, Project Genomics Evidence Neoplasia Information Exchange (GENIE) y The Cancer Genome Atlas (TCGA) en casi 300 pacientes con glioma, 206 de los cuales eran adultos. Analizaron la información clínica, incluidos los tratamientos que recibieron los pacientes y cuánto tiempo vivieron, y la estructura y composición molecular de los tejidos tumorales, incluidas las alteraciones genéticas. Dividieron los tumores en tres grupos, en función de cómo la alteración BRAF activa una vía de señalización llamada ERK (quinasa regulada por señales extracelulares) que contribuye al cáncer: Clase I (mutaciones como BRAFv600E en la que BRAF es capaz de activar ERK por sí mismo), Clase II (mutaciones en las que BRAF necesita emparejarse con otra molécula BRAF para activar ERK en un proceso llamado dimerización), Clase III (mutaciones que amplifican la señalización de ERK a través del gen RAS y otras moléculas de señalización), así como reordenamientos, amplificaciones y otras alteraciones no clasificadas de genes.
La Dra. Schreck dice que descubrió que los gliomas alterados por BRAF en adultos y niños tenían características diferentes. Había más BRAF Clase Iv600E alteraciones en los adultos y más fusiones BRAF en el glioma infantil (la fusión ocurre cuando parte de un gen BRAF se une incorrectamente o se «fusiona» con un gen diferente, lo que permite que cause cáncer). BRAFv600E las alteraciones se asociaron con una mejor supervivencia general en adultos con glioma, pero para el tipo de glioma más agresivo, el glioblastoma, esa mejoría desapareció, y el aumento de la edad se asoció con una peor supervivencia en estos pacientes.
Los investigadores también encontraron que BRAFv600E confirió sensibilidad a la terapia dirigida en pacientes adultos. Sabían que el glioma con BRAFv600E las alteraciones pueden ser sensibles al tratamiento con inhibidores de BRAF y MEK. Este estudio mostró que los pacientes que recibieron estos tratamientos vivieron más que aquellos con la misma alteración BRAF y grado tumoral que no los recibieron. También demostraron que había otras alteraciones de BRAF en pacientes con glioma que podrían tratarse con inhibidores de MEK o inhibidores de BRAF que alteran la dimerización. Esperan que este estudio motive a los investigadores a incluir el glioma con estas mutaciones en los ensayos clínicos que evalúan nuevos fármacos inhibidores de BRAF.
Las terapias dirigidas detuvieron el crecimiento o redujeron el glioma en seis de los 13 pacientes adultos tratados con ellas; seis pacientes tenían xantoastrocitoma pleomórfico, cuatro tenían glioblastoma multiforme, dos tenían astrocitoma pilocítico y uno tenía otro tipo de astrocitoma. El tiempo promedio (mediana) antes de que el cáncer progresara fue de cinco meses y el tiempo de supervivencia general fue de casi 14 años. Fueron cuatro años y medio en pacientes con glioblastoma.
La Dra. Schreck concluye que ella y sus colegas han encontrado una amplia gama de alteraciones genéticas en este gran grupo de pacientes con gliomas que conducen a BRAF. Ella dice que los hallazgos sugieren que existen características biológicas distintas que pueden influir en los resultados clínicos y que deben estudiarse más a fondo para comprender su impacto.
La profesora Ruth Plummer, de la Universidad de Newcastle, Reino Unido, es presidenta del 34º Simposio EORTC-NCI-AACR y no participó en la investigación. Ella dijo: «Estos resultados muestran cómo los gliomas pueden comportarse de manera diferente en adultos y niños, lo que podría incluir cómo responden a las terapias dirigidas. El estudio avanza en lo que sabemos sobre los gliomas en adultos y este conocimiento nos permitirá adaptar mejor los tratamientos al cáncer. dependiendo de las variaciones específicas en el gen BRAF. También nos permitirá desarrollar nuevas y mejores terapias para abordar diferentes variaciones genéticas. El glioma puede ser una enfermedad difícil de tratar con éxito y necesitamos urgentemente encontrar nuevos medicamentos que nos ayuden a mejorar los resultados. para estos pacientes».
Un biomarcador predictivo de respuesta a la terapia en pacientes con cáncer colorrectal metastásico microsatélite estable
Más información:
Resumen n.º 3, «Análisis clínico y molecular integrado del glioma con mutación BRAF en adultos», por Karisa Schreck, presentado en la sesión plenaria 3, de 10:00 a 11:30 h CEST, jueves 27 de octubre, Sala 111 + 112.
Proporcionado por la Organización Europea para la Investigación y el Tratamiento del Cáncer
Citación: Las alteraciones específicas en el gen BRAF pueden afectar la respuesta al tratamiento y la supervivencia en cánceres de cerebro en adultos (26 de octubre de 2022) consultado el 26 de octubre de 2022 de https://medicalxpress.com/news/2022-10-specific-braf-gene-affect- respuesta.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.