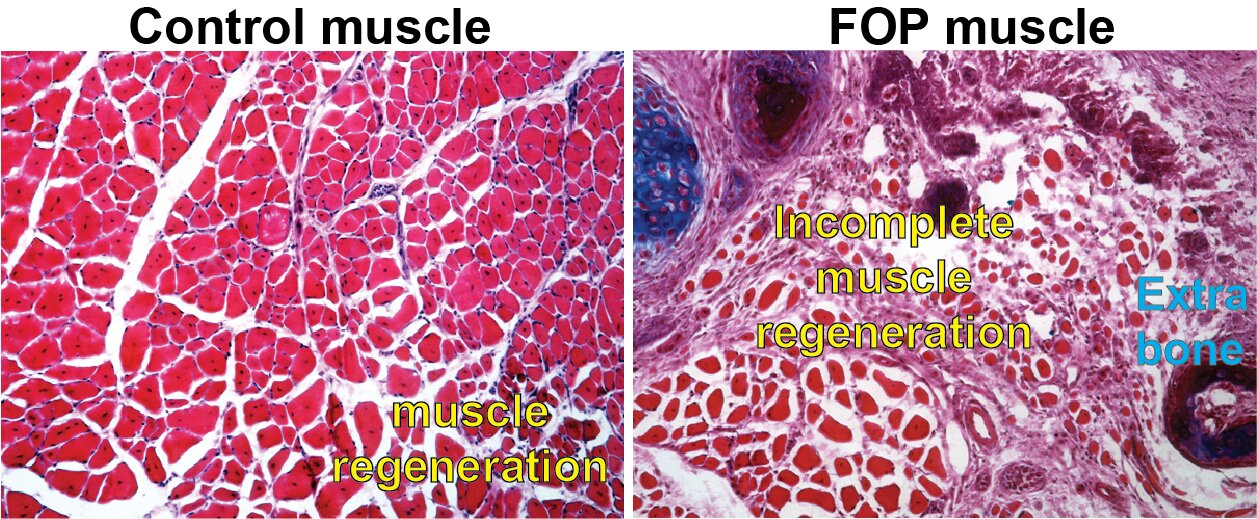
Una imagen de una célula de control con regeneración muscular normal comparada con una célula con la misma mutación genética que tienen las personas con FOP. Crédito: Medicina Penn
La fibrodisplasia osificante progresiva (FOP) es una enfermedad rara caracterizada por un crecimiento óseo extenso fuera del esqueleto normal que se adelanta a las respuestas normales del cuerpo incluso a lesiones menores. Da como resultado lo que algunos denominan un «segundo esqueleto», que bloquea el movimiento de las articulaciones y podría dificultar la respiración. Sin embargo, una nueva investigación en ratones realizada por un equipo de la Escuela de Medicina Perelman de la Universidad de Pensilvania muestra que la formación de hueso extraesquelético podría no ser el único impulsor de la enfermedad. La regeneración del tejido muscular deteriorada e ineficiente parece abrir la puerta a la formación de hueso no deseado en áreas donde debería aparecer músculo nuevo después de las lesiones. Este descubrimiento abre la posibilidad de buscar nuevas terapias para FOP y fue publicado hoy en npj medicina regenerativa.
«Si bien hemos logrado grandes avances para comprender mejor esta enfermedad, este trabajo muestra cómo la biología básica puede proporcionar grandes conocimientos sobre las terapias de medicina regenerativa apropiadas», dijo el autor principal del estudio, Foteini Mourkioti, Ph.D., profesor asistente de Cirugía Ortopédica. y Biología Celular y del Desarrollo, así como codirector del Programa Musculoesquelético del Instituto Penn de Medicina Regenerativa. «Desde el laboratorio, ahora podemos demostrar que existe potencial para un nuevo campo de terapias para pacientes con esta devastadora condición».
Hace unos 15 años, los investigadores de Penn, incluida la coautora de este estudio, Eileen Shore, Ph.D., profesora de Cirugía Ortopédica y Genética y codirectora del Centro de Investigación de FOP y Trastornos Relacionados, descubrieron que un la mutación en el gen ACVR1 fue responsable de la FOP. En ese estudio, el equipo descubrió que la mutación cambiaba las células dentro de los músculos y los tejidos conectivos, desviando las células dentro del tejido para que se comportaran como células óseas, lo que resultó en hueso extraesquelético nuevo e innecesario dentro del cuerpo.
«Sin embargo, mientras que las investigaciones sobre cómo la mutación FOP altera la regulación de las decisiones sobre el destino de las células se han llevado a cabo extensamente en los últimos años, se ha prestado poca atención a los efectos de la mutación genética en el músculo y su impacto en las células que reparan las lesiones musculares». dijo Shore. «Estábamos convencidos de que seguir investigando en esta área podría proporcionar pistas no solo para prevenir la formación de hueso adicional, sino también para mejorar la función y la regeneración muscular, aportando una nueva claridad a la FOP en su conjunto».
Los investigadores estudiaron el músculo de ratones con la misma mutación en el gen ACVR1 que tienen las personas con FOP. Se centraron en dos tipos específicos de células madre de tejido muscular: progenitores fibroadipogenéticos (FAP) y células madre musculares (MuSC). Por lo general, la reparación de lesiones musculares requiere un equilibrio cuidadoso de estos dos tipos de células. El tejido lesionado responde mediante una expansión de las células FAP, que se asignan para reclutar células madre musculares que regenerarán el tejido muscular dañado. Después de unos tres días, las FAP mueren y su trabajo ha terminado. Al mismo tiempo, las MuSC hacen la transición hacia un estado más maduro y diferenciado, llamado fibra muscular, esencial para el movimiento organizado de nuestros músculos.
En los ratones con la mutación ACVR1 que estudiaron Mourkioti, Shore y sus coautores, la apoptosis, el proceso mediante el cual las células FAP mueren como parte de la regeneración muscular adecuada, se había ralentizado significativamente, lo que llevó a una alta presencia de FAP más allá de su nivel habitual. esperanza de vida. Esto alteró su equilibrio con las MuSC. El tejido lesionado también mostró una capacidad disminuida para la maduración de células madre musculares y, como resultado, las fibras musculares eran considerablemente más pequeñas en ratones que portaban la mutación ACVR1 en comparación con las fibras musculares en ratones sin la mutación.
«La persistencia prolongada de FAP enfermas dentro del músculo en regeneración contribuye al entorno muscular alterado en FOP, lo que reduce la regeneración muscular y permite que los FAP sobreabundantes contribuyan a la formación de hueso extraesquelético», dijo Mourkioti. «Esto proporciona una perspectiva completamente nueva sobre cómo se forma el exceso de hueso extraesquelético y cómo se podría prevenir».
Los objetivos actuales para tratar la FOP se centran en ralentizar el crecimiento óseo extraesquelético. Esta investigación puede proporcionar una nueva dirección fundamental. «Proponemos que las intervenciones terapéuticas deberían considerar promover el potencial de regeneración de los músculos junto con la reducción de la formación de hueso ectópico», escribieron Shore y Mourkioti. «Al abordar tanto las poblaciones de células madre como sus funciones en el origen de la FOP, existe la posibilidad de terapias muy mejoradas».
Otros autores en el estudio incluyen a Alexandra Stanley, Elisia Tichy, Jacob Kocan y Douglas Roberts.
Más información:
Dinámica de las células madre residentes en el músculo esquelético durante la miogénesis en la fibrodisplasia osificante progresiva, npj medicina regenerativa, 2022.
Citación: Origen de la enfermedad rara FOP arraigada en la disfunción de la regeneración muscular (2022, 14 de enero) recuperado el 14 de enero de 2022 de https://medicalxpress.com/news/2022-01-rare-disease-fop-rooted-muscle.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.