Crédito: Investigación de circulación (2023). DOI: 10.1161/CIRCRESAHA.122.321583
Una mayor conciencia y los avances en el tratamiento han mejorado en gran medida las tasas de supervivencia después de un ataque al corazón. Sin embargo, con más sobrevivientes, ha llegado el desafío de manejar los impactos a largo plazo en la función cardíaca, especialmente la insuficiencia cardíaca crónica, en la que el corazón pierde gradualmente su capacidad para bombear sangre.
La mortalidad entre las personas afectadas por insuficiencia cardíaca crónica después de un ataque al corazón (conocido médicamente como infarto de miocardio (IM)) es alta. Pero, según una nueva investigación de un gran esfuerzo colaborativo dirigido por científicos de la Escuela de Medicina Lewis Katz de la Universidad de Temple, es posible que pronto se alcancen tratamientos más efectivos.
El nuevo trabajo se centra en una molécula conocida como factor neurotrófico derivado del cerebro (BDNF), que muestra que la pérdida de BNDF es la base de la insuficiencia cardíaca posterior a un infarto de miocardio. Más significativamente, los investigadores demostraron en animales que los niveles de BDNF se pueden reponer terapéuticamente, eliminando el daño al tejido cardíaco y permitiendo que el corazón se recupere.
«La identificación de BDNF como un objetivo terapéutico es un importante paso adelante en el desarrollo de tratamientos mejorados para la insuficiencia cardíaca», dijo Walter J. Koch, Ph.D., presidente de WW Smith Endowed en Medicina Cardiovascular, profesor y presidente del Departamento. de Farmacología y Director del Centro de Medicina Traslacional de la Facultad de Medicina de Katz, y autor principal del nuevo estudio.
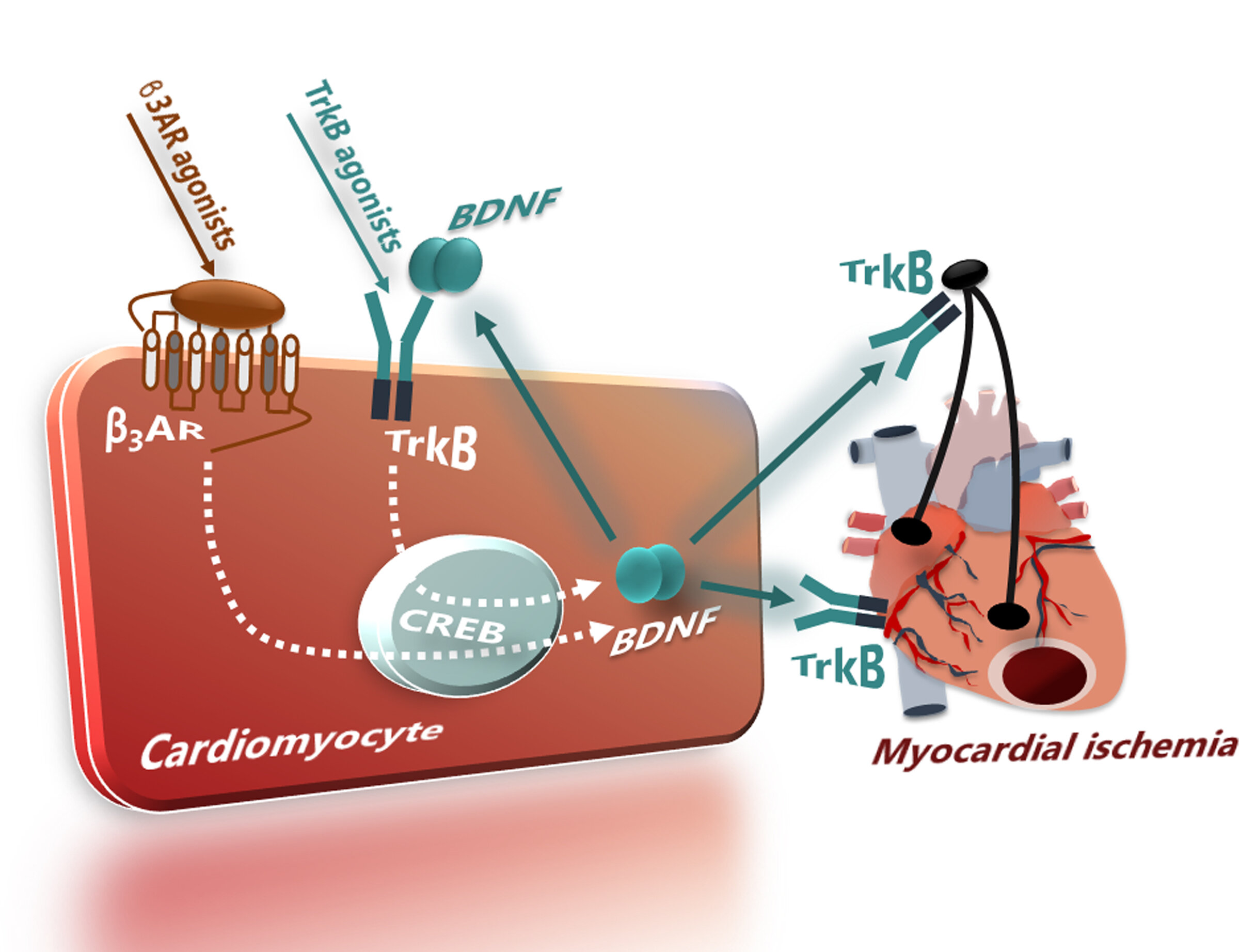
Además de delinear el papel del BDNF, el Dr. Koch y sus colegas muestran por primera vez que la generación reducida de BDNF en el corazón está asociada con la señalización alterada del receptor β-adrenérgico (βAR) y que la estimulación de una proteína conocida como tropomiosina quinasa El receptor B (TrkB) enriquece los niveles de BDNF en el corazón. «Estas acciones combinadas atenúan la progresión de la insuficiencia cardíaca», dijo el Dr. Koch.
Investigadores Nazareno Paolocci, MD, Ph.D., Profesor Asociado de Medicina en la Facultad de Medicina de la Universidad Johns Hopkins, y Alessandro Cannavo, Ph.D., ex becario postdoctoral en el laboratorio del Dr. Koch en Temple y ahora Profesor Asociado en la Universidad de Nápoles Federico II en Italia y autor principal del nuevo informe, colaboró con el Dr. Koch para llevar a cabo el estudio. Los hallazgos del grupo fueron publicados por la revista Investigación de circulación.
Los investigadores comenzaron su investigación examinando los niveles de BDNF en ratones de tipo salvaje cuyos corazones habían estado temporalmente privados de sangre, produciendo un estado conocido como isquemia y, por lo tanto, imitando los efectos de un ataque al corazón. Posteriormente, los ratones desarrollaron insuficiencia cardíaca crónica y luego fueron tratados con un agonista de TrkB. En otra serie de experimentos, los investigadores generaron ratones que carecían de expresión de BDNF en el corazón. Estos ratones knockout para BDNF también se sometieron a isquemia, de forma similar a los ratones de tipo salvaje.
Sabiendo que la estimulación de β3AR también puede enriquecer el BDNF en las células, los investigadores investigaron más a fondo si los efectos de TrkB estaban relacionados con la señalización de βAR. «Los medicamentos que actúan sobre βAR protegen a los pacientes contra un ataque cardíaco, pero se desconoce el mecanismo que utilizan los medicamentos para ejercer sus acciones», explicó el Dr. Koch.
Los experimentos revelaron cambios post-isquémicos en los niveles de BNDF, caracterizados inicialmente por un aumento en BDNF, seguido de una fuerte disminución, y mostraron que la estimulación con TrkB restauró los niveles de BDNF y mejoró la función cardíaca post-isquémica. Estos efectos se vieron reforzados por el enriquecimiento de BDNF en las células cardíacas impulsado por un β3AR, un subtipo distinto de βAR. «La generación de BDNF es otro mecanismo de defensa puesto en marcha por las células del corazón para protegerse contra la isquemia», comentó el Dr. Paolocci.
Aunque se necesita más investigación para comprender mejor si TrkB y β3AR interactúan para generar BDNF, los hallazgos podrían tener implicaciones traslacionales inmediatas. «La estimulación selectiva de β3AR por parte de los agonistas existentes podría adaptarse fácilmente para su uso en pacientes con insuficiencia cardíaca crónica», señaló el Dr. Koch. «Los tratamientos futuros también pueden aprovechar TrkB, que es un objetivo prometedor para el desarrollo de nuevas terapias para la insuficiencia cardíaca».
Más información:
Alessandro Cannavo et al, La generación del factor neurotrófico derivado del cerebro (BDNF) dependiente de β3AR limita la insuficiencia cardíaca posisquémica crónica, Investigación de circulación (2023). DOI: 10.1161/CIRCRESAHA.122.321583
Citación: Los científicos descubren nuevos mecanismos y posibilidades terapéuticas para la insuficiencia cardíaca (30 de marzo de 2023) consultado el 31 de marzo de 2023 en https://medicalxpress.com/news/2023-03-scientists-uncover-mechanisms-therapeutic-possibilities.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.