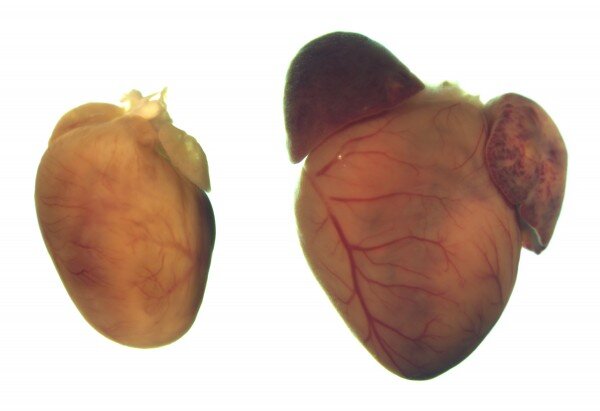
Estos corazones representativos de ratones de 12 semanas de edad muestran un corazón normal (izquierda) y un corazón agrandado que es característico de la miocardiopatía dilatada. Crédito: UT Southwestern Medical Center
Usando el sistema de edición de genes CRISPR-Cas9, los investigadores de UT Southwestern corrigieron las mutaciones responsables de una afección cardíaca hereditaria común llamada miocardiopatía dilatada (DCM) en células humanas y en un modelo de ratón de la enfermedad. Sus hallazgos, publicados en Ciencia Medicina Traslacionalpuede que algún día brinde esperanza a aproximadamente 1 de cada 250 personas en todo el mundo que padecen esta afección.
«Todas las características de la enfermedad que vemos debido a estas mutaciones se revirtieron con la terapia CRISPR-Cas9. Es justo decir que el éxito de este enfoque superó por completo nuestras expectativas», dijo Eric Olson, Ph.D., Presidente y Profesor de Biología Molecular en UTSW, quien codirigió el estudio con sus colegas Rhonda Bassel-Duby, Ph.D., Profesora de Biología Molecular, y Takahiko Nishiyama, MD, Ph.D., becario postdoctoral en el laboratorio de Olson.
La MCD es causada por mutaciones en un gen conocido como proteína 20 con motivo de unión al ARN (RBM20), que afecta la producción de cientos de proteínas en las células del músculo cardíaco responsables de la acción de bombeo del corazón. Esta enfermedad causa estragos generalizados en todo el corazón, destruyendo gradualmente su capacidad para contraerse y causando que se agrande extremadamente y falle con el tiempo. El tratamiento se limita a medicamentos, que pueden mejorar la función contráctil pero no brindan una solución permanente, o un trasplante de corazón, que con frecuencia no es una opción debido a la escasez de órganos de donantes.
Buscando atacar la causa raíz de esta enfermedad, los Dres. Olson, Bassel-Duby, Nishiyama y sus colegas buscaron CRISPR-Cas9, una herramienta popular para la investigación genética reconocida con el Premio Nobel de Química en 2020. Con este sistema, los investigadores pueden corregir potencialmente mutaciones que causan enfermedades en genes importantes.
Hasta el momento, la Administración de Drogas y Alimentos ha aprobado un solo ensayo clínico que utiliza esta tecnología para tratar de tratar la enfermedad de células falciformes. Sin embargo, el Dr. Olson dijo que CRISPR-Cas9 tiene un enorme potencial para tratar una cantidad incalculable de otras enfermedades genéticas. El Dr. Olson y sus colegas han utilizado la edición de genes CRISPR para desarrollar una técnica para detener la progresión de la distrofia muscular de Duchenne en modelos animales.
Para determinar la viabilidad de este enfoque para DCM, el equipo de investigación utilizó un virus para administrar componentes CRISPR-Cas9 a las células del músculo cardíaco derivadas de células humanas que portan dos tipos diferentes de mutaciones que causan DCM. Los científicos utilizaron esta tecnología de edición de genes para intercambiar un solo nucleótido, la unidad básica del ADN, para corregir un tipo de mutación. En otro conjunto de células, los investigadores reemplazaron una pieza de ADN de RBM20 mutado con un segmento sano de este gen.
Después del tratamiento con CRISPR-Cas9, las células mutantes perdieron gradualmente las características inherentes a la DCM: la proteína producida por RBM20 se movió a su lugar normal en el núcleo y las células comenzaron a producir proteínas saludables.
Cuando los investigadores administraron el tratamiento CRISPR-Cas9 a ratones de 1 semana de edad que portaban una de estas mutaciones, los animales nunca desarrollaron corazones agrandados y tuvieron una esperanza de vida normal. Los ratones no tratados tenían síntomas similares a los de los pacientes humanos con DCM.
Los científicos dijeron que quedan varios desafíos antes de que esta terapia pueda usarse en pacientes con DCM. Es necesario trabajar para garantizar que los efectos de CRISPR-Cas9 sean permanentes y precisos, y que se administre la menor dosis posible. También se determinará si el tratamiento podría usarse en pacientes cuya enfermedad está más avanzada. Sin embargo, el Dr. Olson dijo que es optimista de que este sistema podría usarse para tratar una variedad de otras enfermedades familiares.
«El ritmo de este campo es realmente impresionante», dijo. «Espero que si esto avanza hacia los pacientes, no estaremos hablando dentro de décadas, estamos hablando dentro de años».
Takahiko Nishiyama et al, La edición genómica precisa de mutaciones patogénicas en RBM20 rescata la miocardiopatía dilatada, Ciencia Medicina Traslacional (2022). DOI: 10.1126/scitranslmed.ade1633
Citación: La terapia génica corrige la mutación responsable de una afección cardíaca común, muestra una investigación (21 de diciembre de 2022) consultado el 22 de diciembre de 2022 en https://medicalxpress.com/news/2022-12-gene-therapy-mutation-responsible-common.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.