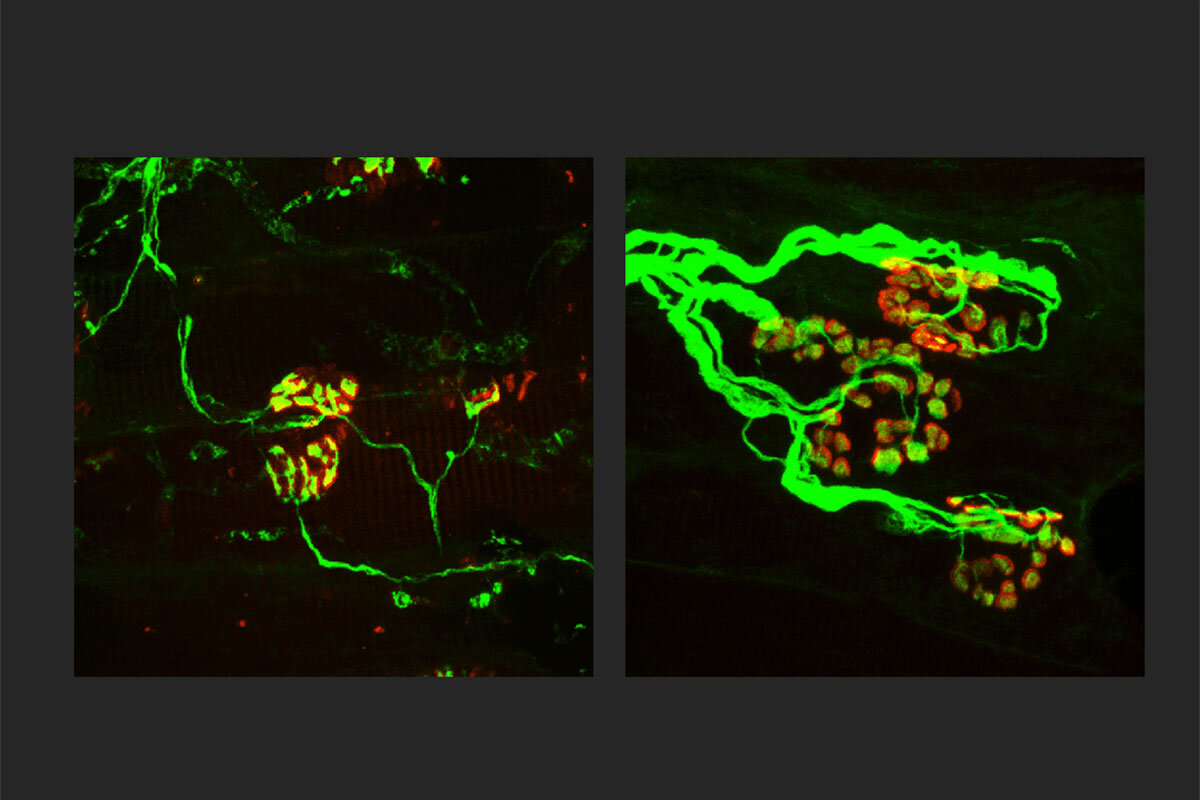
Investigadores de la Facultad de Medicina de la Universidad de Washington en St. Louis están trabajando en un tratamiento para las enfermedades neurodegenerativas que se dirige a SARM1, una molécula clave en la muerte de los axones, el cableado del sistema nervioso. En la imagen, los axones (verde) son más delgados en un modelo de roedor de una neuropatía periférica axonal hereditaria (izquierda). Cuando falta SARM1 en roedores con el trastorno, los axones son más gruesos (derecha) e indistinguibles de los axones normales y sanos. Encontrar formas de bloquear SARM1 podría conducir a nuevas terapias para una amplia gama de enfermedades neurodegenerativas. Crédito: Yurie Yamada
Dos nuevos estudios de la Facultad de Medicina de la Universidad de Washington en St. Louis respaldan el desarrollo de un tratamiento ampliamente aplicable para las enfermedades neurodegenerativas que se dirige a una molécula que sirve como ejecutor central en la muerte de los axones, el cableado del sistema nervioso.
El bloqueo de este verdugo molecular previene la pérdida de axones, que se ha implicado en muchas enfermedades neurodegenerativas, desde neuropatías periféricas hasta la enfermedad de Parkinson y desde el glaucoma hasta la esclerosis lateral amiotrófica (ELA).
Los nuevos estudios, ambos publicados el 26 de octubre en la Revista de investigación clínica, revelan detalles sorprendentes sobre cómo la molécula, llamada SARM1, desencadena la muerte del axón que subyace en el desarrollo de enfermedades neurodegenerativas. La investigación también apunta a nuevos enfoques terapéuticos para enfermedades definidas por la pérdida de axones.
«Necesitamos desesperadamente tratamientos para las enfermedades neurodegenerativas», dijo el coautor principal Jeffrey Milbrandt, MD, Ph.D., profesor James S. McDonnell y director del Departamento de Genética. «Con la evidencia del papel central de SARM1 en estas enfermedades, estamos muy interesados en encontrar formas de bloquear esta molécula, ya sea con inhibidores de moléculas pequeñas o técnicas de terapia génica. Nuestra investigación más reciente sugiere que también podemos interferir con su capacidad para impulsar la neuroinflamación dañina. Tenemos la esperanza de que este trabajo conduzca a nuevas terapias efectivas en una variedad de enfermedades neurodegenerativas y neuroinflamatorias».
En 2017, Milbrandt y el coautor principal Aaron DiAntonio, MD, Ph.D., Profesor Alan A. y Edith L. Wolff de Biología del Desarrollo, descubrieron que SARM1 es una enzima que puede promover la neurodegeneración. Poco después, cofundaron una empresa emergente llamada Disarm Therapeutics para impulsar el desarrollo de compuestos farmacológicos que inhiben el SARM1 para el tratamiento de enfermedades caracterizadas por la degeneración del axón. En 2020, Eli Lilly and Company adquirió Disarm Therapeutics para promover el desarrollo de terapias dirigidas a SARM1 para enfermedades neurodegenerativas.
En las neuronas sanas, SARM1 siempre está apagado. Pero después de una lesión o debido a una enfermedad, SARM1 se activa. El SARM1 activado es un pirómano: quema tanta energía celular que los axones no pueden sobrevivir. Esta crisis energética desencadena la desintegración de los axones.
Para comprender más sobre el papel de SARM1 en el desencadenamiento de la destrucción del axón, los investigadores estudiaron un síndrome de neuropatía progresiva misterioso y extremadamente raro, tan raro que carece de nombre. Esta rara enfermedad resultó ser un buen modelo para comprender el papel del sistema inmunitario en las enfermedades neuroinflamatorias en general. Al secuenciar los genomas de los pacientes, los investigadores encontraron que la pérdida de axones fue causada por errores genéticos en el gen. NMNAT2, cuya función normal mantiene SARM1 apagado. Debido a estos errores genéticos, SARM1 se activa constantemente, lo que desencadena la destrucción de axones. Los investigadores utilizaron la técnica de edición de genes CRISPR para reproducir estas mutaciones en ratones. Al igual que las personas con el síndrome, estos ratones sobrevivieron hasta la edad adulta, pero empeoraron la disfunción motora, la pérdida de axones periféricos y, lo que es más importante, una infiltración de células inmunitarias llamadas macrófagos.
Los investigadores se sorprendieron al descubrir que la reducción del número de macrófagos revirtió la pérdida de axones y los síntomas de la enfermedad en los ratones. El estudio sugiere que SARM1 no solo contribuye directamente a la pérdida de axones, sino que también desempeña un papel en la conducción de la neuroinflamación que solo sirve para agravar los problemas. Los hallazgos también sugieren que algunas afecciones neurodegenerativas podrían tratarse con fármacos inmunomoduladores que bloquean los macrófagos u otras células inmunitarias inflamatorias.
En el segundo artículo, los investigadores investigaron el posible papel de SARM1 en la enfermedad de Charcot-Marie-Tooth tipo 2a, una forma común de neuropatía periférica hereditaria y un buen modelo para estudiar la pérdida de axones en general. Los pacientes con esta enfermedad tienen una pérdida progresiva de axones motores y sensoriales y desarrollan dificultad para caminar, debilidad muscular y sensación de hormigueo o ardor en las manos y los pies. La enfermedad es causada por una mutación en una proteína importante en las mitocondrias, las fábricas de energía de las células. La mutación, en una proteína llamada mitofusin2, afecta la función normal de las mitocondrias. Mucha investigación se ha centrado en las mitocondrias anormales, asumiendo que deben ser la raíz del problema en esta enfermedad.
Sorprendentemente, los investigadores descubrieron que la eliminación de SARM1 en un modelo de roedor con la enfermedad de Charcot-Marie-Tooth tipo 2a detuvo la mayoría de los problemas que presentaban los animales, independientemente de las mitocondrias enfermas. Eliminando la muerte axonal bloqueada o ralentizada por SARM1, la atrofia muscular, las anomalías mitocondriales y los problemas con las uniones neuromusculares, donde las neuronas interactúan con el músculo. Incluso con la proteína mutante mitofusin2 presente, la eliminación de SARM1 protegió a las mitocondrias de una mayor degradación y disfunción.
«Cuando bloqueamos SARM1, no solo protegemos los axones, sino que obtenemos mitocondrias mucho más saludables», dijo DiAntonio. «Fue una completa sorpresa, pero esperamos que pueda ser relevante en muchas enfermedades neurodegenerativas donde el daño mitocondrial es central, como la enfermedad de Parkinson, ya que muchas enfermedades neurodegenerativas tienen un componente de disfunción mitocondrial».
La clave molecular puede desbloquear nuevos tratamientos para los trastornos neurodegenerativos
Yurie Yamada et al, Un circuito de retroalimentación mitocondrial/SARM1 impulsa la neuropatogénesis en un modelo de rata con enfermedad de Charcot-Marie-Tooth tipo 2A, Revista de investigación clínica (2022). DOI: 10.1172/JCI161566
Citación: Nueva estrategia muestra potencial para bloquear la pérdida de nervios en enfermedades neurodegenerativas (27 de octubre de 2022) consultado el 27 de octubre de 2022 en https://medicalxpress.com/news/2022-10-strategy-potential-block-nerve-loss.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.