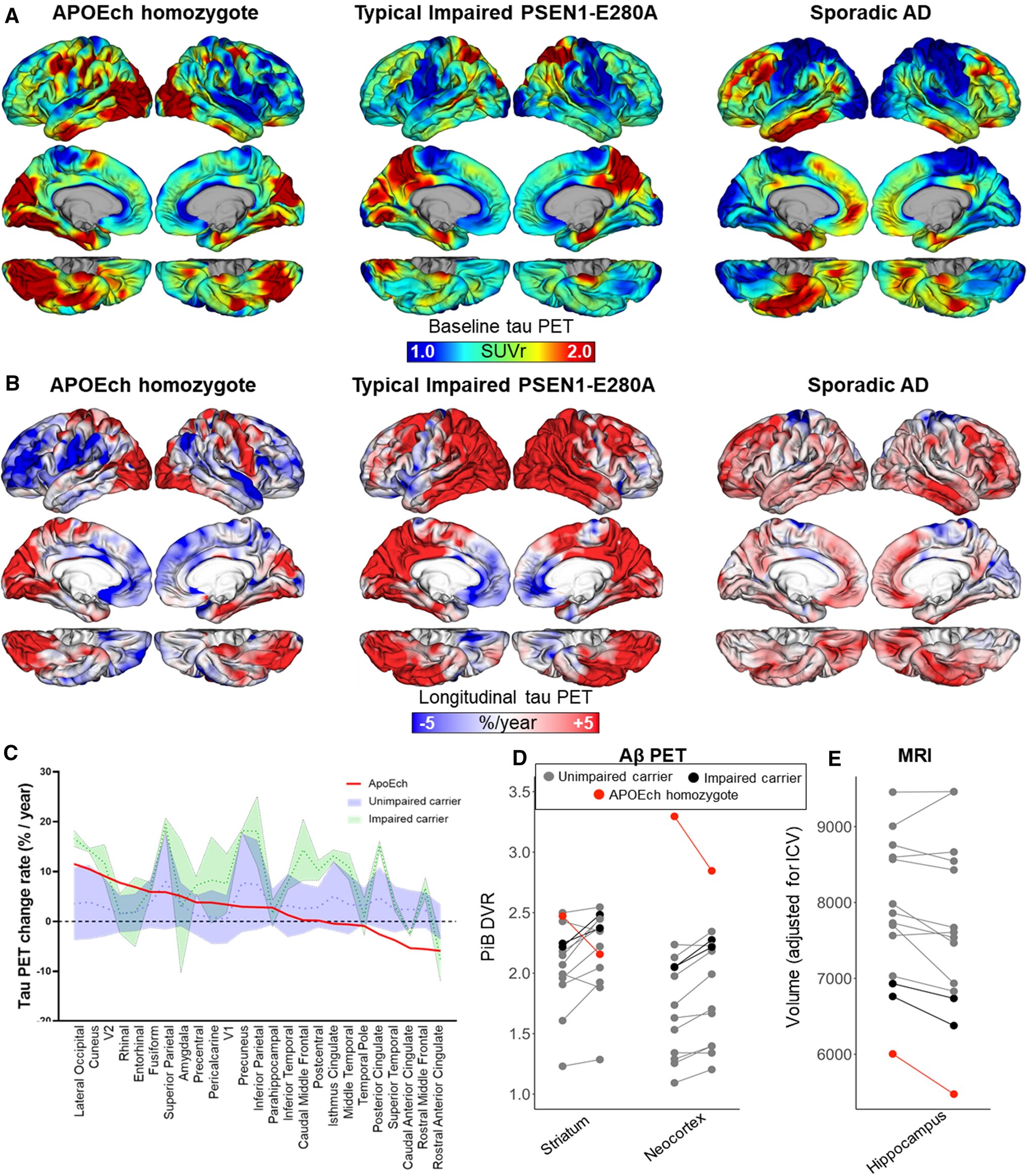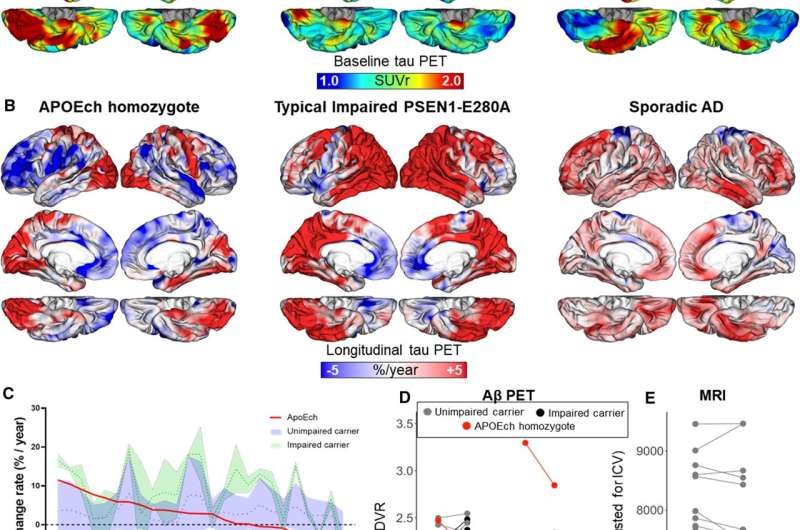
Medidas longitudinales de imágenes PET de tau en un homocigoto APOE3ch. A Representación de superficie de imágenes PET de tau (Flortaucipir) (relación de valor de captación estandarizada, SUVr), al inicio, seguimiento de 3 años (centro) y tasa de cambio B (expresada como %/año), en el homocigoto APOE3ch, (izquierda) un portador deteriorado PSEN1-E280A típico (centro) y un caso AD esporádico (derecha). C Gráfica del área de distribución que muestra las tasas de cambio porcentual anualizadas en tau PET para homocigotos APOE3ch (línea roja) en relación con portadores de PSEN1-E280A no deteriorados (azul) y deteriorados (verde). Las regiones a lo largo del eje x están ordenadas de la tasa de cambio más alta a la más baja observada en el homocigoto APOE3ch. D Diagramas de espagueti de las mediciones de Aβ PET (Pittsburgh Compound B, PiB) al inicio ya los 2 años de seguimiento, E Mediciones de resonancia magnética estructural al inicio y 2 años de seguimiento del volumen del hipocampo. Crédito: Acta neuropatológica (2022). DOI: 10.1007/s00401-022-02467-8
Aliria Rosa Piedrahita de Villegas debió haber desarrollado la enfermedad de Alzheimer a los 40 y murió a causa de la enfermedad a los 60 debido a una rara mutación genética.
En cambio, vivió sin demencia hasta los 70 años, y ahora su cerebro está arrojando pistas importantes sobre la patología de la demencia y los posibles tratamientos para la enfermedad de Alzheimer.
Como investigadores del Hospital General de Massachusetts (MGH) y otros centros describieron por primera vez en 2019, la mujer, de Medellín, Colombia, era miembro de una familia extensa con una mutación en un gen llamado PSEN1.
La mutación PSEN1 E280A es autosómica dominante, lo que significa que solo se requiere una única copia del gen para causar la enfermedad.
Los portadores de la mutación suelen mostrar síntomas de Alzheimer a los 40 o 50 años, y mueren a causa de la enfermedad poco después, pero esta mujer no comenzó a mostrar signos de Alzheimer hasta los 70 años. Murió en 2020 de melanoma metastásico a la edad de 77 años.
“Este es un caso pionero para la enfermedad de Alzheimer y ya ha abierto nuevos caminos para el tratamiento y la prevención, que actualmente estamos siguiendo con algunos colaboradores. Este trabajo ahora está sacando a la luz algunos de los mecanismos de resistencia de la enfermedad de Alzheimer”, dice investigador Yakeel T. Quiroz, Ph.D.
Quiroz es director del Programa Multicultural de Prevención del Alzheimer (MAPP) en Mass General, Profesor Asociado de Psicología en el Departamento de Psiquiatría de la Facultad de Medicina de Harvard y Paul B. y Sandra M. Edgerley MGH Research Scholar 2020–2025.
La diferencia clave en la capacidad de la mujer colombiana para defenderse de la enfermedad durante tres décadas parecía ser que, además de tener la mutación PSEN1 E280A, también era portadora de ambas copias de una mutación conocida como APOE3 Christchurch.
La familia de genes APOE controla la producción de apolipoproteínas, que transportan lípidos (grasas) en la sangre y otros fluidos corporales.
Se sabe que la variante APOE2 protege contra la demencia de Alzheimer, mientras que la variante APOE4 está relacionada con un mayor riesgo de padecer la enfermedad.
APOE3, la variante más común, generalmente no se asocia con un riesgo reducido o aumentado de Alzheimer.
Como Quiroz y sus colegas informan ahora en la revista de neuropatología Acta neuropatológicala mujer, de hecho, tenía características patológicas de la enfermedad de Alzheimer en su cerebro, pero no en las regiones del cerebro donde se encuentran típicamente las características de la enfermedad de Alzheimer.
«Este paciente nos dio una ventana a muchas fuerzas en competencia (acumulación anormal de proteínas, inflamación, metabolismo de lípidos, mecanismos homeostáticos) que promueven o protegen contra la progresión de la enfermedad y comienzan a explicar por qué algunas regiones del cerebro se salvaron mientras que otras no», dice. Justin Sanchez, AB, coautor e investigador de MGH Neurology.
Los investigadores identificaron en el cerebro de Aliria un patrón distinto de agregación anormal o «agrupamiento» de tau, una proteína que se sabe que está alterada en la enfermedad de Alzheimer y otros trastornos neurológicos.
En este caso, la patología tau salvó en gran medida la corteza frontal, que es importante para el juicio y otras funciones «ejecutivas», y el hipocampo, que es importante para la memoria y el aprendizaje.
En cambio, la patología tau involucró la corteza occipital, el área del cerebro en la parte posterior de la cabeza que controla la percepción visual.
La corteza occipital fue la única región cerebral importante que exhibió las características típicas de la enfermedad de Alzheimer, como la inflamación crónica de las células cerebrales protectoras llamadas microglía y niveles reducidos de expresión de APOE.
«Por lo tanto, la variante de Christchurch puede afectar la distribución de la patología tau, modula la edad de inicio, la gravedad, la progresión y la presentación clínica de [autosomal dominant Alzheimer’s disease]lo que sugiere posibles estrategias terapéuticas», escriben los investigadores.
«Es raro que tengamos sorpresas agradables al estudiar los cerebros de la enfermedad de Alzheimer familiar. Este caso mostró un fenotipo protegido sorprendentemente claro. Estoy seguro de que nuestros hallazgos moleculares y patológicos al menos sugerirán algunas vías de investigación y generarán la esperanza de un tratamiento exitoso contra este trastorno», dice el coprimer autor, Diego Sepúlveda-Falla, MD, líder de investigación en el Centro Médico Universitario de Hamburgo-Eppendorf en Hamburgo, Alemania.
“Este caso excepcional es un experimento diseñado por la naturaleza que nos enseña una forma de prevenir el Alzheimer: observemos, aprendamos e imitemos a la naturaleza”, concluye el Dr. Francisco Lopera, director del Grupo de Neurociencias de Antioquia en Medellín, Colombia. Lopera es coautora principal y la neuróloga que descubrió a esta familia y la ha estado siguiendo durante los últimos 30 años.
La variante genética puede ayudar a proteger contra la enfermedad de Alzheimer
Diego Sepúlveda-Falla et al, Neuropatología tau distinta y perfiles celulares de un homocigoto de Christchurch APOE3 protegido contra la demencia de Alzheimer autosómica dominante, Acta neuropatológica (2022). DOI: 10.1007/s00401-022-02467-8
Citación: Un cerebro que desafía al Alzheimer ofrece pistas para el tratamiento y la prevención de la demencia (28 de julio de 2022) recuperado el 28 de julio de 2022 de https://medicalxpress.com/news/2022-07-alzheimer-defying-brain-clues-treatment-dementia .html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.