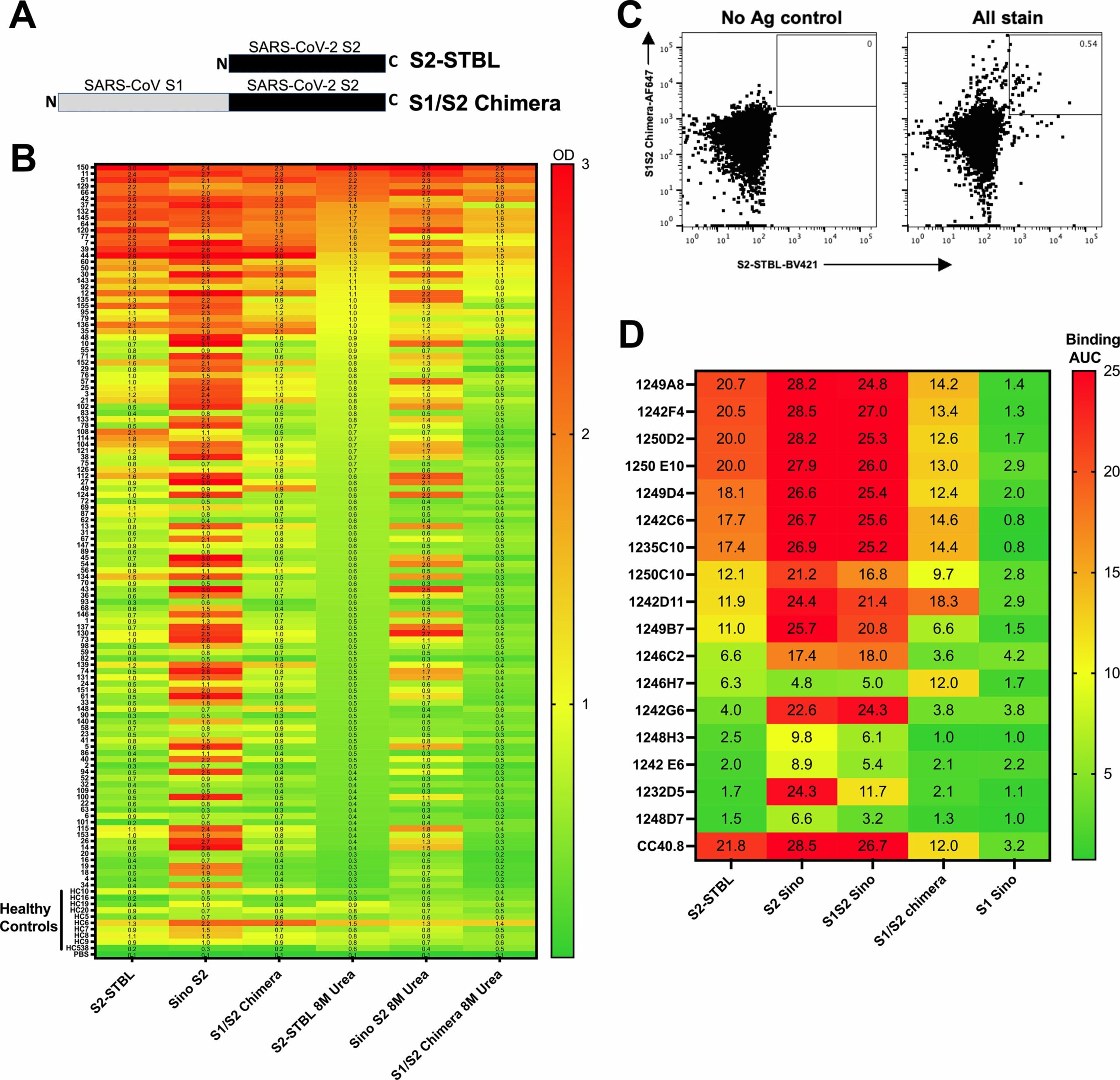
Aislamiento de anticuerpos monoclonales humanos (hmAbs) específicos de SARS-CoV-2 S2. (A) Representación esquemática de las proteínas quiméricas S2-STBL y S1/S2 utilizadas como cebos para ELISA y citometría de flujo. (B) El plasma humano de sujetos sanos o convalecientes se diluyó 1:1000 en PBS y se analizó por duplicado en un ELISA frente a las proteínas indicadas; Se muestra la absorbancia a 450 nM. Cada fila es un tema individual. (C) Estrategia de activación representativa para el aislamiento de células B S2+. Las parcelas iniciales están cerradas en células B CD3-CD4-CD14-anexinV-CD19+CD27+ vivas. (D) los hmAb se analizaron a 10 y 1 μg/ml por duplicado mediante ELISA para determinar la unión a la proteína indicada; se indica el área bajo la curva (AUC). Crédito: Patógenos PLOS (2022). DOI: 10.1371/journal.ppat.1010691
El SARS-CoV-2 que causa el COVID-19 ha matado a 6,3 millones de personas en todo el mundo desde 2019, lo que destaca dolorosamente la vulnerabilidad de la humanidad a los nuevos coronavirus.
Los investigadores descubrieron un anticuerpo monoclonal neutralizante que potencialmente actúa como una potente terapia universal contra el coronavirus contra el SARS-CoV-2 y todas sus variantes preocupantes, incluidas beta, gamma, delta, epsilon y omicron. También muestra efectividad contra los mortales coronavirus anteriores SARS-CoV, el Síndrome Respiratorio Agudo Severo que surgió en China en 2002, y MERS-CoV, el Síndrome Respiratorio de Medio Oriente que apareció en Arabia Saudita en 2012. Incluso muestra efectividad contra varios comunes coronavirus fríos.
Esta actividad universal contra todos los beta-coronavirus resulta de un anticuerpo monoclonal que se dirige a la región del tallo S2 de la proteína del pico viral (S) que está altamente conservada entre los beta-coronavirus, pero que también es esencial para que el virus se adhiera e ingrese a las células, lo que lleva a infección.
En experimentos con animales, el anticuerpo monoclonal protegió contra infecciones cuando se administró como una inyección intraperitoneal o una dosis nasal. El estudio se publica en la revista Patógenos PLOS por los coautores principales James J. Kobie, Ph.D., y Mark R. Walter, Ph.D., de la Universidad de Alabama en Birmingham, y Luis Martinez-Sobrido, Ph.D., de Texas Biomedical Research Instituto, San Antonio, Texas.
El anticuerpo monoclonal y otro anticuerpo monoclonal descubierto anteriormente por los investigadores se están desarrollando como un cóctel terapéutico para COVID-19 bajo licencia de Aridis Pharmaceuticals, una compañía biofarmacéutica de California.
El objetivo general de los investigadores de la UAB, el Instituto de Investigación Biomédica de Texas y Aridis es encontrar anticuerpos que no permitan el escape inmunológico de las variantes mutadas del SARS-CoV-2, el virus que causa el COVID-19. Esto incluye omicron y cualquier variante futura de interés. Se espera que la identificación y el estudio de dichos anticuerpos puedan conducir al desarrollo de vacunas que protejan de todos los coronavirus.
«El SARS-CoV-2 marca la tercera vez en las últimas dos décadas que un beta-coronavirus causa una mortalidad significativa en humanos», dijo Kobie. «El SARS-CoV-2 ha causado la mayor cantidad de infecciones y muertes en todo el mundo. Las nuevas variantes presentan el riesgo de evadir el sistema inmunitario, incluso en personas vacunadas y previamente infectadas, y existe la posibilidad de que surjan otros coronavirus genéticamente distintos como nuevas cepas pandémicas. en el futuro.»
«Por estas razones, encontrar nuevos medicamentos terapéuticos y profilácticos y estrategias de vacunas que tengan una actividad universal contra el coronavirus es esencial para proteger a la humanidad contra los brotes o pandemias actuales y futuros de beta-coronavirus».
Las vacunas y otros anticuerpos monoclonales contra el SARS-CoV-2 se han centrado en gran medida en el dominio de unión al receptor, o RBD, ubicado en las cabezas del pico de la proteína viral S que se proyecta desde la superficie del virus. Cada virus tiene de 24 a 40 picos. El RBD es muy bueno para provocar una respuesta inmune, pero esa parte de la S permite muchas mutaciones que pueden permitir que el virus escape de los anticuerpos.
Una clave en la presente investigación fue encontrar un objetivo de anticuerpo en una parte de la espiga llamada S2, o la región del tallo. Esta región está altamente conservada y rara vez muta porque eso interrumpiría su función esencial. Después de que el RBD en la cabeza de la S une el coronavirus a una molécula receptora en la superficie de una célula objetivo, el tallo S2 actúa para llevar el virus al interior de la célula objetivo. Allí, el virus se replica, matando a la célula y liberando una gran cantidad de nuevos viriones infecciosos.
La búsqueda de anticuerpos útiles comenzó con el análisis de muestras de sangre de pacientes adultos convalecientes en el UAB Hospital a través del UAB COVID Enterprise Biorepository dirigido por Paul Goepfert, MD, y Nathaniel Erdmann, MD, Ph.D., División de Enfermedades Infecciosas de la UAB. Las células B de memoria en la sangre que se unieron a los cebos de proteína S2 personalizados, desarrollados por Walter para imitar el estado natural del dominio S2 del pico, se usaron para crear un panel de células únicas capaces de producir anticuerpos monoclonales humanos, o hmAbs, que luego podrían ser examinados para determinar su eficacia contra el virus. Las células de memoria que se dirigen a S2 son escasas porque el RBD es inmunodominante; sus diversos sitios antigénicos representan el 90 por ciento de la actividad neutralizante del plasma convaleciente.
Diecisiete hmAbs mostraron unión a la proteína S2. Solo cuatro de estos pudieron neutralizar un pseudovirus SARS-CoV-2 y un SARS-CoV-2 vivo, incluidas las variantes beta y omicron.
El de mejor desempeño, el hmAb 1249A8, tuvo la actividad neutralizante más amplia y potente contra cepas que incluían el SARS-CoV-2 original de Wuhan, China; las variantes beta, gamma, delta, epsilon y omicron; el SARS-CoV y MERS-CoV; y dos virus del resfriado común.
El hmAb protegió a los ratones de la enfermedad por SARS-CoV-2, según lo medido por el mantenimiento del peso corporal y la eliminación del virus de los pulmones del ratón cuatro días después de la infección. Además, el hmAb 1249A8 mostró sinergia cuando se usó en combinación con 1213H7, otro hmAb descubierto por los investigadores. 1213H7 es activo contra el RBD de la glicoproteína S viral.
En colaboración con Aridis, que se especializa en la administración respiratoria de anticuerpos monoclonales para tratar infecciones, los investigadores habían demostrado previamente que la administración respiratoria directa de un hmAb 1213H7 específico de SARS-CoV-2 RBD permite una actividad terapéutica sustancial de ahorro de dosis en hámsters. Por lo tanto, los investigadores evaluaron este mecanismo de administración para el tratamiento del SARS-CoV-2 y el SARS-CoV con el hmAb 1249A8 específico de S2 y el hmAb 1213H7.
El cóctel 1249A8, 1213H7, administrado como dosis nasal, 12 horas después de las infecciones con SARS-CoV-2 delta o el primer SARS-CoV aislado en 2002, tuvo una amplia actividad terapéutica en hámsters.
«Estos resultados indican la cooperatividad in vivo entre los hmAb neutralizantes específicos de S1 y S2 y que los mAb neutralizadores de coronavirus universales potentes con potencial terapéutico pueden inducirse en humanos y pueden guiar el desarrollo de una vacuna universal contra el coronavirus», dijo Kobie.
«Se han aprobado numerosos hmAbs específicos de SARS-CoV-2 RBD para uso clínico. Desafortunadamente, varios se han vuelto irrelevantes debido a su incapacidad para neutralizar variantes preocupantes, incluido el omicron más reciente, lo que destaca el peligroso futuro de las terapias de mAb basadas solo en RBD contra el coronavirus».
Aridis está utilizando los dos hmAb en su cóctel AR-701 diseñado para administración por inhalación. AR-701 está diseñado para una eficacia de acción prolongada, que puede durar un año o más cuando se usa en humanos.
Demostración preclínica de una potente terapia universal de anticuerpos monoclonales contra el coronavirus para todas las variantes de COVID-19
Michael S. Piepenbrink et al, Potente actividad terapéutica universal de beta-coronavirus mediada por la administración respiratoria directa de un anticuerpo monoclonal neutralizante humano específico del dominio Spike S2, Patógenos PLOS (2022). DOI: 10.1371/journal.ppat.1010691
Citación: Demostración de una potente terapia universal de anticuerpos monoclonales contra el coronavirus para todas las variantes de COVID-19 (21 de julio de 2022) consultado el 21 de julio de 2022 en https://medicalxpress.com/news/2022-07-potent-universal-coronavirus-monoclonal- anticuerpo.html
Este documento está sujeto a derechos de autor. Aparte de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin el permiso por escrito. El contenido se proporciona únicamente con fines informativos.